网址:http://m.1010jiajiao.com/timu3_id_340945[举报]
业已发现许多含金的化合物可以治疗风湿症等疾病,引起科学家广泛兴趣。在吡啶(![]() )的衍生物2,2'-联吡啶(代号A)中加入冰醋酸与30% H2O2的混合溶液,反应完成后加入数倍体积的丙酮,析出白色针状晶体B(分子式C10H8N2O2)。B的红外光谱显示它有一种A没有的化学键。B分成两份,一份与HAuCl4在温热的甲醇中反应得到深黄色沉淀C。另一份在热水中与NaAuCl4反应,得到亮黄色粉末D。用银量法测得C不含游离氯而D含游离氯7.18%。C的紫外光谱在211nm处有吸收峰,与B的213nm特征吸收峰相近,而D则没有这一吸收。C和D中金的配位数都是4。
)的衍生物2,2'-联吡啶(代号A)中加入冰醋酸与30% H2O2的混合溶液,反应完成后加入数倍体积的丙酮,析出白色针状晶体B(分子式C10H8N2O2)。B的红外光谱显示它有一种A没有的化学键。B分成两份,一份与HAuCl4在温热的甲醇中反应得到深黄色沉淀C。另一份在热水中与NaAuCl4反应,得到亮黄色粉末D。用银量法测得C不含游离氯而D含游离氯7.18%。C的紫外光谱在211nm处有吸收峰,与B的213nm特征吸收峰相近,而D则没有这一吸收。C和D中金的配位数都是4。
5-1 画出A、B、C、D的结构式。
5-2 在制备B的过程中加入丙酮起什么作用?
5-3 给出用游离氯测定值得出D的化学式的推理和计算的过程。 查看习题详情和答案>>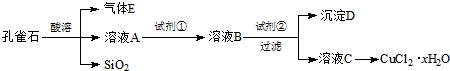
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀的pH | 2.7 | 5.4 | 8.1 |
| 沉淀完全的pH | 3.7 | 6.9 | 9.6 |
A.Ca(ClO)2 B.H2O2 C.HNO3 D.KMnO4
反应的离子方程式为
(2)加入试剂②的目的是调节pH至a,a的范围是
(3)为了测定制得的氯化铜晶体(CuCl2?xH2O)中x值,有同学设计了如下实验方案:称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是
.某课外活动小组用铜屑制取五水合硫酸铜晶体。已知硫酸铜和硝酸铜的溶解度数据如下表:
T/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
硫酸铜/g | 14.8 | 20.5 | 28.5 | 39.6 | 53.6 | 73.0 |
硝酸铜/g | 83.5 | 125.0 | 163.0 | 182.0 | 208.0 | 247.0 |
⑴课外活动小组设计的实验步骤如下:
①用灼烧法除去铜屑表面的有机物和油污。灼烧时需要使用到的仪器有 ▲ 。
A.烧杯 B.酒精灯 C.泥三角 D.蒸发皿 E.坩埚 F.漏斗
②将灼烧后的固体置于烧杯中,向其中加入一定量的硫酸,将烧杯放置在通风橱中加热,并向其中分批加入适量浓硝酸,直至反应结束,滤去少量不溶物。发生反应的化学方程式为: ▲ 。
③将所得滤液用水浴加热蒸发浓缩,待看到 ▲ 时,停止加热,冷却过滤得硫酸铜晶体。本操作采用水浴加热的原因 ▲ 。
④除去硫酸铜晶体中含有的少量硝酸铜。可以用 ▲ 法提纯硫酸铜晶体。
⑵该活动小组设计的制备硫酸铜晶体的实验方案,主要存在问题是消耗的酸多、产生的气体污染空气。请你重新设计一种经济、环保的实验方案: ▲ 。
二茂铁(结构如图)是一个典型的金属有机化合物,实验室常用氯化亚铁和环戊二烯在碱性条件下反应得到。反应原理为:FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O
二茂铁的熔点为172~173℃,在100℃开始升华。能溶于乙醚、二甲亚砜等非极性溶剂,不溶于水,对碱和非氧化性酸稳定。制备的步骤如下:
步骤1.在150mL的三颈瓶中加入25g细粉末状KOH和60mL无水乙醚,通入氮气并搅拌约10分钟使之尽可能溶解,然后加入5.5 mL环戊二烯,再搅拌10分钟。
步骤2. 向烧杯中加入25 mL二甲亚砜和6.5g新制的无水氯化亚铁,微热至40℃并搅拌使其溶解,然后加入滴液漏斗中。
步骤3. 按图所示的装置装配好仪器,打开滴液漏斗的活塞,缓慢将氯化亚铁等加入三颈瓶中,并继续搅拌1小时。
步骤4. 反应结束后,将混合物倒入100mL 18%的盐酸溶液,将烧杯放在冰浴中冷却,搅拌约10分钟,使结晶完全。
步骤5. 抽滤,将获得的产品以冷水洗涤2~3次,低温风干得到粗制的二茂铁。
(1)步骤1中通入N2的目的可能是 。
(2)步骤2中,滴液漏斗侧边的玻璃导管的作用是 。
(3)实验装置中,冷凝管通水,水应从 口进(选填a或b)。
(4)步骤4将反应后的混合物倒入盐酸中,发生主要反应的离子方程式是 。
(5)步骤5用冷水洗涤是因为 ,因此可采用 的方法,进一步提纯二茂铁。
查看习题详情和答案>>
二茂铁(结构如图)是一个典型的金属有机化合物,实验室常用氯化亚铁和环戊二烯在碱性条件下反应得到。反应原理为:FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O
二茂铁的熔点为172~173℃,在100℃开始升华。能溶于乙醚、二甲亚砜等非极性溶剂,不溶于水,对碱和非氧化性酸稳定。制备的步骤如下:
步骤1.在150mL的三颈瓶中加入25g细粉末状KOH和60mL无水乙醚,通入氮气并搅拌约10分钟使之尽可能溶解,然后加入5.5 mL环戊二烯,再搅拌10分钟。
步骤2. 向烧杯中加入25 mL二甲亚砜和6.5g新制的无水氯化亚铁,微热至40℃并搅拌使其溶解,然后加入滴液漏斗中。
步骤3. 按图所示的装置装配好仪器,打开滴液漏斗的活塞,缓慢将氯化亚铁等加入三颈瓶中,并继续搅拌1小时。
步骤4. 反应结束后,将混合物倒入100mL 18%的盐酸溶液,将烧杯放在冰浴中冷却,搅拌约10分钟,使结晶完全。
步骤5. 抽滤,将获得的产品以冷水洗涤2~3次,低温风干得到粗制的二茂铁。
(1)步骤1中通入N2的目的可能是 。
(2)步骤2中,滴液漏斗侧边的玻璃导管的作用是 。
(3)实验装置中,冷凝管通水,水应从 口进(选填a或b)。
(4)步骤4将反应后的混合物倒入盐酸中,发生主要反应的离子方程式是 。
(5)步骤5用冷水洗涤是因为 ,因此可采用 的方法,进一步提纯二茂铁。
查看习题详情和答案>>