28.(12分)为了防止环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以制取高浓度的SO2和(NH4)2SO4和NH4HSO4固体。
为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出。[(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
|
实验序号 |
样品的质量/g |
NaOH溶液的体积/mL |
氨气的体积/L |
|
Ⅰ |
7.4 |
40.00 |
1.68 |
|
Ⅱ |
14.8 |
40.00 |
3.36 |
|
Ⅲ |
22.2 |
40.00 |
1.12 |
|
Ⅳ |
37.0 |
40.00 |
0.00 |
(1)上述实验过程中有关反应的离子方程式为: , 。
(2)由Ⅰ组数据直接推测:标准状况下3.7g样品进行同样实验时,求生成氨气的体积。
(3)试计算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比。
(4)欲计算该NaOH溶液的物质的量浓度应选择第 组数据,求NaOH溶液的物质的量浓度。
答案:选择题1-19题
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
B |
C |
C |
C |
C |
B |
C |
D |
C |
D |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
|
|
AC |
B |
CD |
B |
AD |
D |
AB |
AC |
BD |
|
 2NaNO2+O2↑ (2)2Cu(NO3)3
2NaNO2+O2↑ (2)2Cu(NO3)3
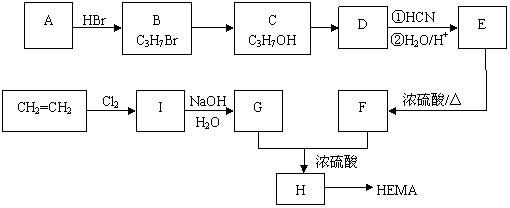
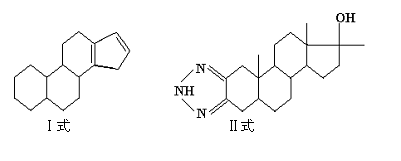 25.(7分)在今年的雅典的奥运会上,奥委会医学委员会明确的提出:类固醇是违禁药物之一,从化学的结构上看,类固醇是一类含有环戊烷多氢菲核基本结构的化合物(I式),只所以属违禁药物,是因为它是一种一烷基化睾酮衍生物,如康力龙其结构式见II式。由于分子中烷基的作用,此种药物对肝功能有明显的副作用。过量服用还会产生女子男性化、肝中毒甚至肝癌等副作用。已知:丁二烯可发生反应:CH2=CH-CH=CH2+Br2
→CH2BrCH=CHCH2Br
25.(7分)在今年的雅典的奥运会上,奥委会医学委员会明确的提出:类固醇是违禁药物之一,从化学的结构上看,类固醇是一类含有环戊烷多氢菲核基本结构的化合物(I式),只所以属违禁药物,是因为它是一种一烷基化睾酮衍生物,如康力龙其结构式见II式。由于分子中烷基的作用,此种药物对肝功能有明显的副作用。过量服用还会产生女子男性化、肝中毒甚至肝癌等副作用。已知:丁二烯可发生反应:CH2=CH-CH=CH2+Br2
→CH2BrCH=CHCH2Br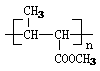
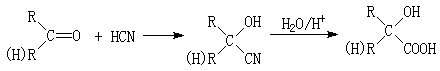

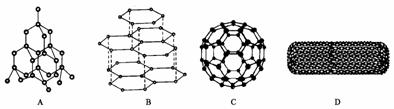
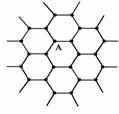 (3)由右边石墨的晶体结构俯视图可推算在石墨晶体中,每个正六边形平均所占有的C 原子数与C-C键数之比为______________________。
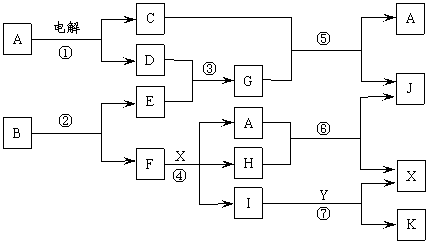
(3)由右边石墨的晶体结构俯视图可推算在石墨晶体中,每个正六边形平均所占有的C 原子数与C-C键数之比为______________________。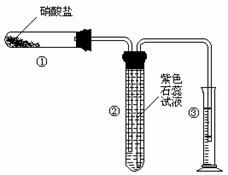 21.(12分)某校化学兴趣小组的同学对硝酸盐的受热分解进行探究。他们设计了如下装置分别加热了NaNO3、Cu(NO3)2、AgNO3。(加热及夹持装置未画出)
21.(12分)某校化学兴趣小组的同学对硝酸盐的受热分解进行探究。他们设计了如下装置分别加热了NaNO3、Cu(NO3)2、AgNO3。(加热及夹持装置未画出)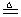 2Ag2O+4NO2↑+O2↑,(Ⅱ) 2AgNO3
2Ag2O+4NO2↑+O2↑,(Ⅱ) 2AgNO3