电解食盐水: 2NaCl + 2H2O == 2NaOH + H2↑ +Cl2↑ 铁与Cl2反应:2Fe+3Cl2===2FeCl3
Cl2 与 水:Cl2+H2O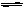 HCl+HClO
Cl2与NaOH:Cl2 +2NaOH=== NaCl+NaClO +H2O
HCl+HClO
Cl2与NaOH:Cl2 +2NaOH=== NaCl+NaClO +H2O
碘的提取: 2KI + C12 ==2KCl + I2 钠与水反应:2Na+2H2O=2NaOH+H2↑
碳酸钠与碳酸氢钠的性质比较
|
溶解性 |
易溶(同温下,溶解度大于碳酸氢钠) |
易溶 |
|
热稳定性 |
稳定 |
2NaHCO3△Na2CO3+CO2↑+H2O
|
|
碱性 |
碱性(相同浓度时,碳酸钠水溶液的PH比碳酸氢钠的大) |
碱性 |
|
盐酸 |
生成CO2 |
生成CO2 比碳酸钠与盐酸反应剧烈 |
碳酸钠与碳酸氢钠鉴别
固体:加热产生气体的是NaHCO3 溶液:加BaCl2产生沉淀的是Na2CO3
Al与强碱反应 2Al + 2 NaOH + 2H2O===2NaAlO2+3H2↑(唯一的一个)
氧化铝(Al2O3):溶于强碱Al2O3 + 2 NaOH = 2NaAlO2 + H2O
离子方程式 Al2O3 + 2OH-= 2AlO2-+ H2O 氢氧化铝和强碱反应 Al(OH)3 + NaOH = NaAlO2 + 2H2O
Fe3+检验:溶液中加入KSCN Fe3++3SCN一══Fe(SCN)3
Cl2与FeCl2反应:2FeCl2+Cl2==2FeCl3
FeCl3 与铁反应 : 2FeCl3 +Fe==3FeCl2
FeCl3 与铜反应:Cu+2FeCl3==CuCl2+2FeCl2
钢铁:电化学腐蚀,碳铁形成原电池
金属防腐的方法1.表面覆盖保护层, 2.改变内部结构; 3. 电化学保护法
SiO2与碱反应:SiO2+2NaOH==Na2SiO3+H2O 实验室装NaOH的试剂瓶用橡皮塞不用玻璃塞
二氧化硅的用途:SiO2是制造光导纤维的主要原料
硅酸盐工业:水泥的原料是黏土和石灰石 玻璃的原料是纯碱、石灰石和石英, (都有石灰石)
|
|
C与浓 H2SO4反应:C+2H2SO4(浓)====CO2↑+2SO2↑+2H2O
铵盐的性质:①易溶于水②与碱反应放出氨气③受热易分解④与碱反应放出氨气
HNO3强氧化性: Cu + 4HNO3(浓) = Cu(NO3)2 + 2NO2 + 2H2O
3Cu + 8HNO3(稀) = 3Cu(NO3)2 + 2NO + 4H2O
C + 4HNO3(浓) = CO2 + 4NO2 + 2H2O
钝化作用:常温下, 浓HNO3使Fe、Al钝化。
 石油的裂解已成为生产乙烯的主要方法
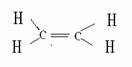
石油的裂解已成为生产乙烯的主要方法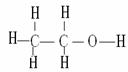 乙烯分子式:C2H4 结构简式:CH2==CH2 结构式
乙烯分子式:C2H4 结构简式:CH2==CH2 结构式 加成反应:CH2=CH2+H2O
加成反应:CH2=CH2+H2O CH3CH2OH CH2=CH2+Br2→CH2BrCH2Br
CH3CH2OH CH2=CH2+Br2→CH2BrCH2Br
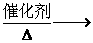 2CH3CHO
+ 2H2O
2CH3CHO
+ 2H2O CH3COOCH2CH3 + H2O
CH3COOCH2CH3 + H2O 


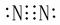
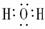
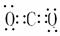 物质的电子式:N2
CO2
H2O
物质的电子式:N2
CO2
H2O
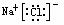
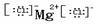 NaOH Na+
NaOH Na+ (2)NaCl:
(2)NaCl:
 非金属性逐渐增强
非金属性:Cl>S>P>Si,
非金属性逐渐增强
非金属性:Cl>S>P>Si,