24.(09江苏卷 17)(8分)废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
17)(8分)废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
 (1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是(填字母)。
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是(填字母)。
 A.热裂解形成燃油
B.露天焚烧
A.热裂解形成燃油
B.露天焚烧
 C.作为有机复合建筑材料的原料 D.直接填埋
C.作为有机复合建筑材料的原料 D.直接填埋
 (2)用
(2)用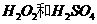 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
的混合溶液可溶出印刷电路板金属粉末中的铜。已知:

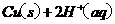 ====
====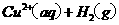
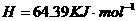

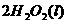 ====
====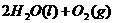
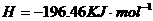

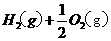 ====
====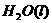
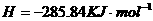
 在
在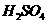 溶液中
溶液中 与
与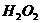 反应生成
反应生成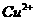 和
和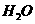 的热化学方程式为。
的热化学方程式为。
 (3)控制其他条件相同,印刷电路板的金属粉末用10℅
(3)控制其他条件相同,印刷电路板的金属粉末用10℅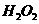 和3.0
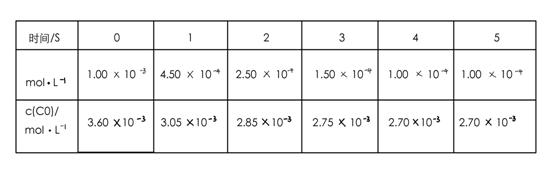
和3.0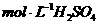 的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。
的混合溶液处理,测得不同温度下铜的平均溶解速率(见下表)。



|
温度(℃) |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
铜平均溶解速率 ( (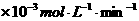 ) ) |
7.34 |
8.01 |
9.25 |
7.98 |
7.24 |
6.73 |
5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是。
 (4)在提纯后的
(4)在提纯后的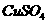 溶液中加入一定量的
溶液中加入一定量的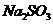 和
和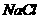 溶液,加热,生成
溶液,加热,生成 沉淀。制备
沉淀。制备 的离子方程式是。
的离子方程式是。
 答案:
答案:
(1)BD
 (2)Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1
(2)Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ.mol-1
 (3)H2O2分解速率加快
(3)H2O2分解速率加快
 (4)2Cu2++SO32-+2Cl-+H2O
(4)2Cu2++SO32-+2Cl-+H2O 2CuCl↓+SO42-+2H+
2CuCl↓+SO42-+2H+
 解析:
解析:
(1)有关环保的比较容易。
(2)主要考察盖斯定律的灵活运用。适当变形,注意反应热的计算。不要忽视热化学方程式的书写的注意事项。
(3)考察影响化学反应速率的因素,结合双氧水的性质即可得出答案。
(4)根据题目条件书写离子方程式常规题。
23.(09安徽卷28) (17分)
(17分)
 Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好PH和
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好PH和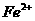 浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。

 [实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
 (1)请完成以下实验设计表(表中不要留空格)。
(1)请完成以下实验设计表(表中不要留空格)。
实验 编号 编号 |
实验目的 |
T/K |
PH |
c/10-3mol·L-1 |
|
|
H2O2 |
Fe2+ |
||||
|
① |
为以下实验作参考 |
298 |
3 |
6.0 |
0.30 |
|
② |
探究温度对降解反应速率的影响 |
|
|
|
|
|
③ |
 |
298 |
10 |
6.0 |
0.30 |
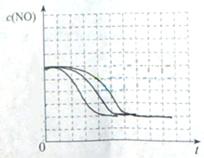
 [数据处理]实验测得p-CP的浓度随时间变化的关系如右上图。
[数据处理]实验测得p-CP的浓度随时间变化的关系如右上图。
 (2)请根据右上图实验①曲线,计算降解反应在50~150s内的反应速率:
(2)请根据右上图实验①曲线,计算降解反应在50~150s内的反应速率:

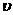 (p-CP)=mol·L-1·s-1
(p-CP)=mol·L-1·s-1
 [解释与结论]
[解释与结论]
 (3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:。
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:。
 (4)实验③得出的结论是:PH等于10时,。
(4)实验③得出的结论是:PH等于10时,。
 [思考与交流]
[思考与交流]
 (5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:
 答案:
答案:
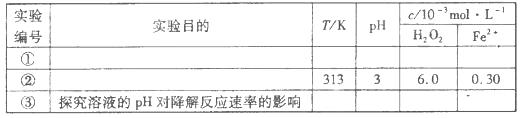
 (1)
(1)

 (2)8.0×10-6
(2)8.0×10-6
 (3)过氧化氢在温度过高时迅速分解。
(3)过氧化氢在温度过高时迅速分解。
 (4)反应速率趋向于零(或该降解反应趋于停止)
(4)反应速率趋向于零(或该降解反应趋于停止)
 (5)将所取样品迅速加入到一定量的NaOH溶液中,使pH约为10(或将所取样品骤冷等其他合理答案均可)
(5)将所取样品迅速加入到一定量的NaOH溶液中,使pH约为10(或将所取样品骤冷等其他合理答案均可)
 解析:
解析:
(1)实验①是参照实验,所以与实验①相比,实验②和③只能改变一个条件,这样才能起到对比实验的目的,则实验②是探究温度对反应速率的影响,则T=313K,pH=3,c(H2O2)=6.0mol·L-1,c(Fe2+)=0.30mol·L-1,实验③显然是探究pH的大小对反应速率的影响;
(2)在50-150s内,△c(p-CP)=0.8mol·L-1,则v(p-CP)=0.08mol·L-1·s-1;(3)温度过高时,H2O2分解,c(H2O2)浓度减小,导致反应速率减小;
(4)从图中看出,pH=10时,c(p-CP)不变,即反应速率为零,说明碱性条件下,有机物p-CP不能降解;
(5)从第(4)可以得出,在发言液中加入NaOH溶液,使溶液的pH迅速增大,反应停止。
 。
。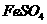 溶液与稍过量的
溶液与稍过量的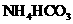 溶液混合,得到含
溶液混合,得到含 的浊液
的浊液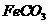 固体
固体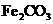 固体
固体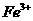 ,该反应的离子方程式是
,该反应的离子方程式是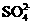 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 ,现煅烧464.0kg的
,现煅烧464.0kg的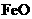 ,则该产品中
,则该产品中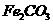 的质量是kg(摩尔质量/g·
的质量是kg(摩尔质量/g·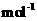 ;
;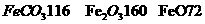 )
)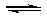 Fe(OH)2+2H+的平衡向逆反应方向移动,从而抑制FeSO4的水解
Fe(OH)2+2H+的平衡向逆反应方向移动,从而抑制FeSO4的水解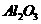 ,含
,含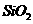 、
、 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下: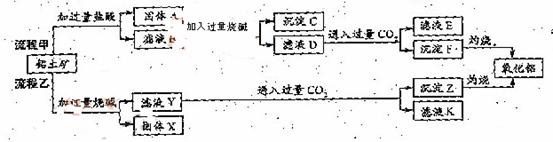
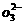 的离子方程式为________.
的离子方程式为________. 的容度积常数
的容度积常数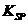 =5.6×
=5.6×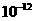 ,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的
,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的 =_______.
=_______. 2Al3++3H2O
2Al3++3H2O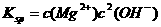 ,
,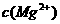 =5.6×10-12/(0.1)2=5.6×10-10。
=5.6×10-12/(0.1)2=5.6×10-10。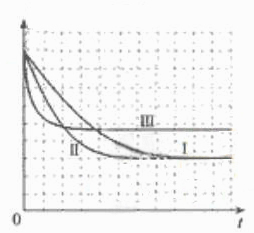
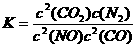 =
= =5000。
=5000。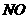 会破坏臭氧层。科学家正在研究利用催化技术将尾气中的
会破坏臭氧层。科学家正在研究利用催化技术将尾气中的 转变成
转变成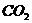 和
和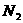 ,化学方程式如下:
,化学方程式如下:
 0(填写“>”、“<”、“=”。
0(填写“>”、“<”、“=”。
 请回答下列问题:
请回答下列问题: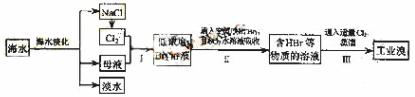
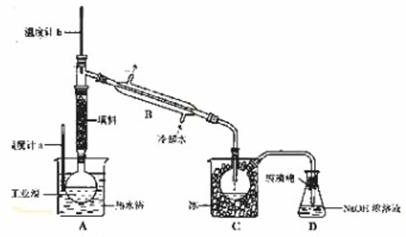

 2NaOH+H2↑+Cl2↑,其中Cl2有可能与NaOH会生成NaClO。步骤I中的Br2的浓度很小,多次用SO2反复吸收,最终用Cl
2NaOH+H2↑+Cl2↑,其中Cl2有可能与NaOH会生成NaClO。步骤I中的Br2的浓度很小,多次用SO2反复吸收,最终用Cl 2处理,则可获得大量的工业溴。溴具有强氧化性可以氧化SO2,生成H2SO4,因此要注意酸对设备的腐蚀问题。溴具有腐蚀性,可以腐蚀橡胶。蒸馏的目的,就是通过沸点不同而提纯Br2,所以要通过温度计控制好Br2沸腾的温度,尽可能使Br2纯净。
2处理,则可获得大量的工业溴。溴具有强氧化性可以氧化SO2,生成H2SO4,因此要注意酸对设备的腐蚀问题。溴具有腐蚀性,可以腐蚀橡胶。蒸馏的目的,就是通过沸点不同而提纯Br2,所以要通过温度计控制好Br2沸腾的温度,尽可能使Br2纯净。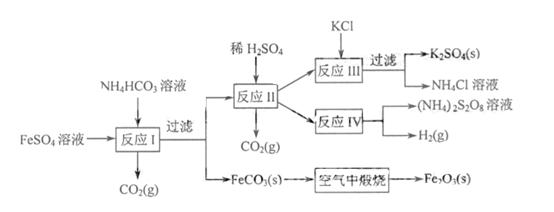
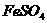 溶液中加入▲(填字母),以除去溶液中的
溶液中加入▲(填字母),以除去溶液中的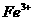 。
。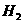
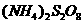 (过二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为。
(过二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为。 液中除去溶液中的
液中除去溶液中的 (3)由题目看出在III反应中生成的K2SO4为固体,而K2SO4在无机溶剂中溶解度是比较大的,要想使K2SO4析出只能降低其溶解度所以加入醇类溶剂目的降低K2SO4的溶解度。
(3)由题目看出在III反应中生成的K2SO4为固体,而K2SO4在无机溶剂中溶解度是比较大的,要想使K2SO4析出只能降低其溶解度所以加入醇类溶剂目的降低K2SO4的溶解度。