15.(10分) 某研究性学习小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
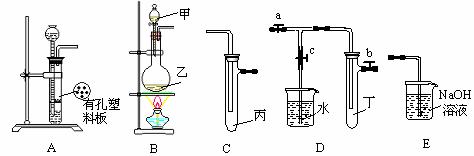
请按要求填空:
(1)利用A装置可制取的气体有
A.用纯碱与稀硫酸反应制CO2 B.用铝合金与氢氧化钠溶液反应制H2
C.用CaC2现水反应制C2H2 D.用硫酸钠与硫酸溶液反应制SO2
(2)A、D、E装置相连后,在A中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验。
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,再打开止水夹 ,使烧杯中的水进入试管丁的操作是 。
②试管丁中的NO2与水充分反应后,若向试管内缓缓通入一定量的O2,直至试管全部充满水,则所得溶液中溶质的物质的量浓度是 (气体按标准状况计算)。
(3)B、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。
① 写出用MnO2和浓盐酸反应制Cl2的离子反应方程式 。
②若在丙中加入适量水,即可制得氯水。将所得氯水分成两份,进行实验I、II两个实验,实验操作、现象、结论如下:
|
实验序号 |
实验操作 |
现象 |
结论 |
|
I |
将氯水滴入品红溶液 |
溶液褪色 |
氯气与水反应的产物有漂白性 |
|
II |
氯水中加入NaHCO3粉末 |
有无色气泡产生 |
氯气与水反应的产物具有较强的酸性 |
③请你评价实验I、II的结论是否合理?若不合理,请说明理由: 。
请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论) 。
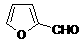
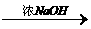
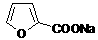
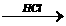
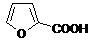

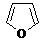

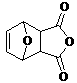
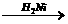
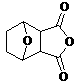
 已知:① 2HCHO+NaOH
CH3OH+HCOONa
已知:① 2HCHO+NaOH
CH3OH+HCOONa (Diels-Alder 反应)
(Diels-Alder 反应)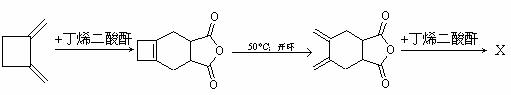
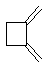 形成高聚物的结构简式:
。
形成高聚物的结构简式:
。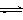 Fe
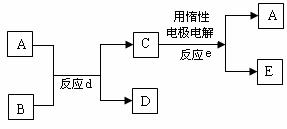
(s)+CO2 (g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
Fe
(s)+CO2 (g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示: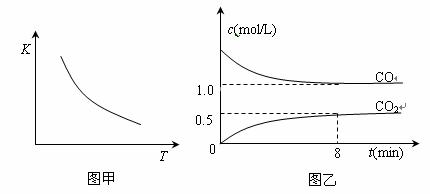

 Na2FeO4+3H2↑。
Na2FeO4+3H2↑。

 xC(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是
xC(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如下图所示。下列说法中正确是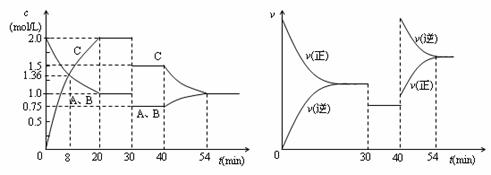
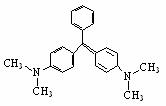 近年来食品安全问题成为社会各界日益关注的焦点话题。香港地区某食物安全中心曾对十五个桂花鱼样本进行化验,结果发现十一个样本中含有孔雀石绿。孔雀石绿是化工产品,具有较高毒性,高残留,且长期服用后,容易致癌、致畸,对人体有害。其结构简式如图所示。
近年来食品安全问题成为社会各界日益关注的焦点话题。香港地区某食物安全中心曾对十五个桂花鱼样本进行化验,结果发现十一个样本中含有孔雀石绿。孔雀石绿是化工产品,具有较高毒性,高残留,且长期服用后,容易致癌、致畸,对人体有害。其结构简式如图所示。 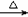 CH2=CH2↑+Br-+H2O
CH2=CH2↑+Br-+H2O