27、(16分)甲、乙、丙均为中学化学常见的气体单质,A、B、C 均为常见的化合物。
已知:①甲、乙生成A是工业生产中常见的反应之一;
②甲与乙在一定条件下反应的有关数据为:
|
物质 |
甲 |
乙 |
A |
|
起始时浓度 |
3 mol•L-1 |
3 mol•L-1 |
0 |
|
2 s 末浓度 |
1.8 mol•L-1 |
2.6 mol•L-1 |
0.8 mol•L-1 |
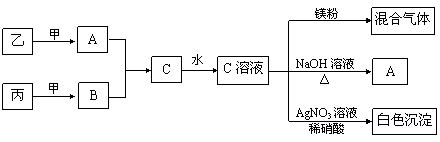 ③ 它们之间存在如下图所示的转化关系:
③ 它们之间存在如下图所示的转化关系:
根据上述信息,回答下列问题:
⑴ 乙的电子式为 ▲ ;
⑵ C晶体中所含的化学键有 ▲ ;
⑶
甲与乙反应的化学方程式为 ▲ ,在前2 s 内甲与乙反应的平均速率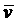 (甲)=
(甲)=
▲ ,2 s末乙的转化率为 ▲ ;
⑷常温下,1g甲在丙中燃烧生成气态B,放出92.3KJ热量,写出该反应的热化学方程式:
▲ ;
⑸ C溶液与镁粉反应生成混合气体的化学式可能为 ▲ ,试分析产生混合气体珠原因 ▲ 。
 ▲ 。
▲ 。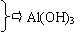 Ⅲ Al→ Al2(SO4)3
Ⅲ Al→ Al2(SO4)3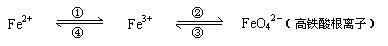
 已知反应2SO2(g)+O2(g) 2SO3(g);△H<0。现有甲、乙两个容积相同的恒容容器。在500℃和有催化剂存在下,向甲中加入2molSO2和1molO2,向乙中加入2molSO3,并同时发生反应。当两容器中反应分别达到平衡后,维持条件不变,则
已知反应2SO2(g)+O2(g) 2SO3(g);△H<0。现有甲、乙两个容积相同的恒容容器。在500℃和有催化剂存在下,向甲中加入2molSO2和1molO2,向乙中加入2molSO3,并同时发生反应。当两容器中反应分别达到平衡后,维持条件不变,则 A.属于芳香族化合物
A.属于芳香族化合物