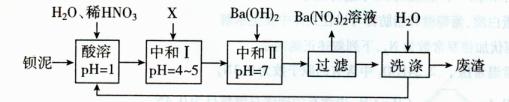
20.(10分)《联合国气候变化框架公约》是世界上第一个为全面控制二氧化碳等温室气体排放,以应对全球气候变暖给人类经济和社会带来不利影响的国际公约。各国科学家们也加强了对CO2创新利用的研究。最近有科学家提出“绿色自由”构想:把空气吹人碳酸钾溶液,然后再把 二氧化碳从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇等。“绿色自由”构想技术流程如下:
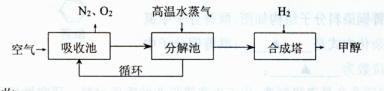
I.二氧化碳的吸收
(1)上述流程中“循环”的意义为 。
(2)吸收池中不用饱和碳酸钠溶液代替饱和碳酸钾溶液可能的原因是 。
(已知:碳酸钾、碳酸钠的价格分别为:5200元/吨、2300元/吨。)
Ⅱ.二氧化碳的利用
(1)2009年我国二氧化碳排放总量约为6.6×109吨,若采用上述流程将二氧化碳转化成甲醇(假设CO2的吸收率为80%,转化率为90%),通过计算确定理论上可制得96c70甲醇多少吨?
(2)工业上常将甲醇加入汽油,制成利于改善城市环境的甲醇汽油。
已知常温下甲醇、汽油及一氧化碳的燃烧热如下:
|
物质 |
甲醇 |
汽油(C8H8) |
一氧化碳 |
|
燃烧热/kJ·mol-l |
725 |
5518 |
283 |
1mol等物质的量的甲醇、汽油(C8 H18)混合的燃料,在一定量的氧气中燃烧,放出热量2980kJ,则反应中生成CO mol。
17.(10分)
(1)已知:N2(g)+ O2(g)=2NO(g) ;△H = 180.5KJ ·mol-l
4NH3(g)+5O2(g)=4NO(g)+6H2O(g);△H= -905KJ·mol-l
2H2(g)+O2(g) =2H2O(g) ;△ H =-483. 6KJ·mol-l
则 N2(g) +3H2(g) 2NH3(g)的△H =
。
2NH3(g)的△H =
。
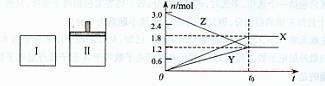
(2)一定温度下在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g) 4NO2(g)+O2(g);△H>O
4NO2(g)+O2(g);△H>O
①反应达到平衡后若再通人一定量氮气,则N2O5的转化率将 (填“增大”、“减小”、“不变”)。
②下表为反应在T,温度下的部分实验数据:
|
时间/S |
0 |
500 |
1000 |
|
c(N2O5)mol·L-1 |
5.00 |
3.52 |
2.48 |
则500s内N2O5的分解速率为 。
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol·L-1,则T2 T1。
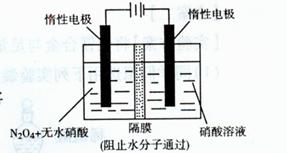
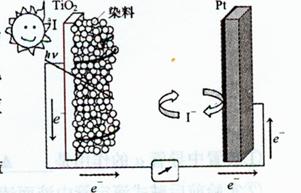
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的 (填“阳极”或“阴极”)区生成,其电极反应式为 。
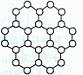 A.(12分)2010年诺贝尔物理学奖授予英国曼彻斯特大学科学家安德烈·海姆和康斯坦丁·诺沃肖洛夫。共同工作多年的二人因“突破性地”用撕裂的方法成功获得超薄材料石墨烯而获奖。制备石墨烯方法有石墨剥离法、化学气相沉积法等。石墨烯的球棍模型示意图如右:
A.(12分)2010年诺贝尔物理学奖授予英国曼彻斯特大学科学家安德烈·海姆和康斯坦丁·诺沃肖洛夫。共同工作多年的二人因“突破性地”用撕裂的方法成功获得超薄材料石墨烯而获奖。制备石墨烯方法有石墨剥离法、化学气相沉积法等。石墨烯的球棍模型示意图如右: 键数为NA
键数为NA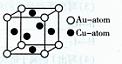 ①钴原子在基态时,核外电子排布式
①钴原子在基态时,核外电子排布式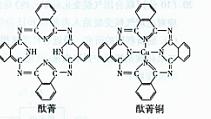 ③金与铜可形成的金属互化物合金(如图),
③金与铜可形成的金属互化物合金(如图), 成一种药物K,其合成路线设计如下:
成一种药物K,其合成路线设计如下: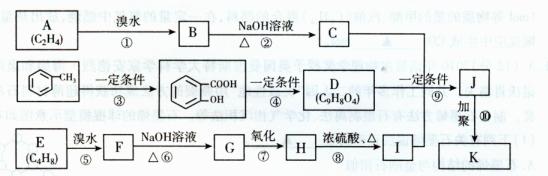
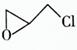 ,则该有机物核磁共振氢谱有 个峰。
,则该有机物核磁共振氢谱有 个峰。 下列说法正确的是
。
下列说法正确的是
。
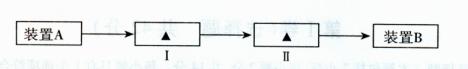
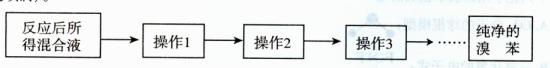
 (14分)某化学课外兴趣小组为探究苯与溴发生反应的反应类型并制取纯净的溴苯,进行如下实验。请根据要求回答相关问题。
(14分)某化学课外兴趣小组为探究苯与溴发生反应的反应类型并制取纯净的溴苯,进行如下实验。请根据要求回答相关问题。