21.(11分)设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) 平衡常数为K1
FeO(s)+CO(g) 平衡常数为K1
反应②Fe(s)+H2O(g)  FeO(s)+H2(g) 平衡常数为K2
FeO(s)+H2(g) 平衡常数为K2
测得在不同温度下,K1、K2值如下:
|
温度/℃ |
K1 |
K2 |
|
500 |
1.00 |
3.15 |
|
700 |
1.47 |
2.26 |
|
900 |
2.40 |
1.60 |
(1)若500℃时进行反应①,CO2起始浓度为2mol.L-1,CO2转化率为____ ▲ _____
(2)反应②在常温下为 ▲ 反应 (填“自发或非自发”)。请简述理由
▲
(3)700℃反应②达到平衡,使得该平衡向右移动,其它条件不变时,可以采取的措施有
_ ▲ (填序号)
A、缩小反应器体积 B、加入水蒸气 C、升高温度到900℃ D、使用合适的催化剂
(4)若反应①在体积固定的密闭容器中进行,在一定条件下达到平衡状态,改变下列条件再达平衡后,相应物质的物理量如何变化?(选填“增大”、“减小”或“不变”)
①降低温度,CO2的平衡浓度 ▲ ;
②再通入CO2,CO2的转化率 ▲ 。
(5)下列图像符合反应①的是 ▲ (填序号)(图中v是速率、φ为混合气体CO含量,T为温度)
17.可逆反应N2(g)+3H2(g)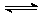 2NH3(g);△H<0,下列研究目的和示意图相符合的是
2NH3(g);△H<0,下列研究目的和示意图相符合的是
|
|
A |
B |
C |
D |
|
研究目的 |
压强对反应的影响(P2>P1) |
温度对反应的影响 |
平衡体系增加N2对反应的影响 |
催化剂对反应的影响 |
|
图示 |
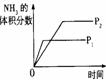 |
 |
 |
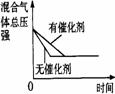 |
 2C(g)达平衡时,A、B、C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是
2C(g)达平衡时,A、B、C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是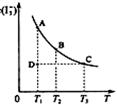 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)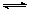 SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是
SO32-+SO2+。若以液态SO2为溶剂,用SOCl2滴定Cs2SO3,则以下叙述错误的是
 C.B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)
△H=-2078 kJ ·molˉ1
C.B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)
△H=-2078 kJ ·molˉ1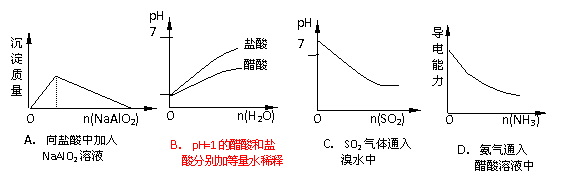
 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH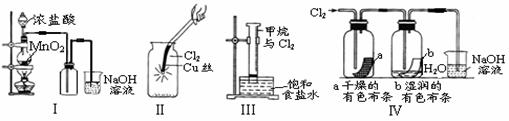
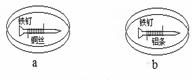 C.a中铜丝上发生氧化反应
C.a中铜丝上发生氧化反应