0 41101 41109 41115 41119 41125 41127 41131 41137 41139 41145 41151 41155 41157 41161 41167 41169 41175 41179 41181 41185 41187 41191 41193 41195 41196 41197 41199 41200 41201 41203 41205 41209 41211 41215 41217 41221 41227 41229 41235 41239 41241 41245 41251 41257 41259 41265 41269 41271 41277 41281 41287 41295 447348
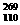 X(暂用X表示),它属于一种新元素-第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒。经分析它属于过渡元素。下列关于该元素的叙述中正确的是 )
X(暂用X表示),它属于一种新元素-第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒。经分析它属于过渡元素。下列关于该元素的叙述中正确的是 )
 CO2+ H2
B.3NO2+H2O=2HNO3+NO
CO2+ H2
B.3NO2+H2O=2HNO3+NO