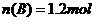(15分)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
16.
 族 族周期 |
IA |
|
0 |
|||||
|
1 |
① |
IIA |
IIIA |
IVA |
VA |
VI |
VIIA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序是 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式: 。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂作为(填序号) 。
a.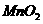 b
b
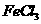 c
c
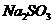 d
d
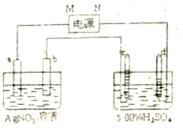
(5)由表中元素形成的常见物质X,Y,Z,M,N可发生以下反应:
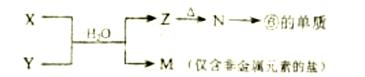
X溶液与Y溶液反应的离子方程式为 ,
N→⑥的单质的化学方程式为 ,
常温下,为使0.1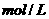
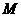 溶液中由M电离的阴,阳离子浓度相等,应向溶液中加入一定量的Y溶液至
。
溶液中由M电离的阴,阳离子浓度相等,应向溶液中加入一定量的Y溶液至
。
 三 (本题包括2小题,共20分)
三 (本题包括2小题,共20分)
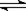 CH3COO-+H+
CH3COO-+H+
 2AlN+3CO合成。下列叙述正确的是
2AlN+3CO合成。下列叙述正确的是
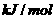 表示。请认真观察反应过程~能量图。然后回答问题
表示。请认真观察反应过程~能量图。然后回答问题 =
(用含
=
(用含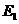 、
、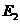 的代数式表示)
的代数式表示)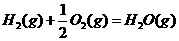
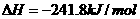 ,该反应的活化能为167.2
,该反应的活化能为167.2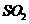 催化氧化成
催化氧化成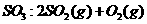

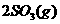
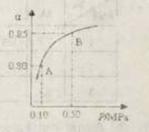 某温度下,
某温度下,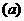 与体系总压强(
与体系总压强(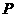 )的关系如图所示,根据图示回答下列问题:
)的关系如图所示,根据图示回答下列问题:

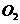 置于10L密闭容器中,
置于10L密闭容器中,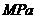 。该反应的平衡
。该反应的平衡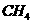 催化还原
催化还原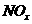 可以消除氮氧化物的污染。例如:
可以消除氮氧化物的污染。例如:

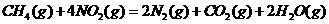
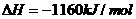
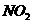 至
至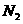 ,整个过程中放出的热量为
,整个过程中放出的热量为 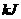 。
。 的溶液100
的溶液100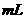
 的试管中放出
的试管中放出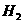 的速率大
的速率大 的速率大
的速率大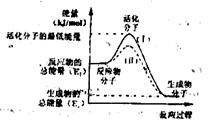 五(本题包括2小题,共12小题)
五(本题包括2小题,共12小题) 和0.55
和0.55 溶液各50mL。
溶液各50mL。 ,中和后生成的溶液的比热容
,中和后生成的溶液的比热容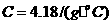 ,反应前后的温度变化为(
,反应前后的温度变化为(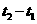 ),中和反应的中和热为:
),中和反应的中和热为: 电极和Pt
电极和Pt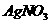 溶液的浓度(填增大,减小或不变,下同) ,
溶液的浓度(填增大,减小或不变,下同) ,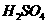 溶液的浓度
,
溶液的浓度
,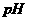 。
。 的化学平衡状态。相关数据如下:
的化学平衡状态。相关数据如下: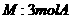
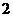
 B, 2min 达到平衡,生成1.2
B, 2min 达到平衡,生成1.2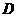 ,测得从反应开始到平衡C的速率为
,测得从反应开始到平衡C的速率为
 ;
;

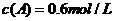 。
。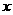 的值可能是3 B.平衡时M中c
的值可能是3 B.平衡时M中c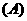 =
=
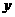 的值可能是1 D.平衡时N中
的值可能是1 D.平衡时N中