18、(10分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为
。
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g),其化学平衡常数K与t的关系如下表:
2NH3(g),其化学平衡常数K与t的关系如下表:
|
t/K |
298 |
398 |
498 |
…… |
|
K/(mol·L-1)-2 |
4.1×106 |
K1 |
K2 |
…… |
请完成下列问题: ①试比较K1、K2的大小,K1 K2(填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是 (填序号字母)。 A.容器内N2、H2、NH3的浓度之比为1:3:2 B.2v(N2)(正)= v(H2)(逆) C.容器内压强保持不变 D.混合气体的密度保持不变 (3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。 ①写出盐酸肼第一步水解反应的离子方程式 。 ②盐酸肼水溶液中离子浓度的关系表示正确的是 (填序号)。 A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-) B.c(Cl-)>c([N2H5·H2O]+)>c(OH-)>c(H+) C.2c(N2H62+)+c([N2H5·H2O]+)+ c(H+) = c(Cl-)+c(OH-) D.c(N2H62+) > c(Cl-)> c(H+) >c(OH-)
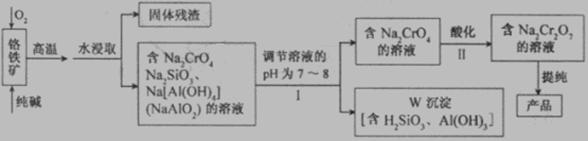 请回答下列问题。
(1)若I中只用一种试剂调节溶液的pH,应选用___________(填标号)。
A.稀硫酸
B.氧化钠固体
C.氢氧化钾溶液
(2)I中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是
_______________________________________________________
(用离子方程式表示)。
(3)Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下: 2CrO42- (黄色)+2H+
请回答下列问题。
(1)若I中只用一种试剂调节溶液的pH,应选用___________(填标号)。
A.稀硫酸
B.氧化钠固体
C.氢氧化钾溶液
(2)I中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是
_______________________________________________________
(用离子方程式表示)。
(3)Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下: 2CrO42- (黄色)+2H+ 试回答:
试回答: 2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。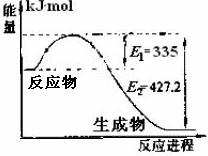 ⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比充入D、E两种气体(此时容器中的气体的总物质的量不要求保持12mol),按D(g)+E(g)
⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比充入D、E两种气体(此时容器中的气体的总物质的量不要求保持12mol),按D(g)+E(g)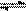 CO(g)+H2O(g)在一定温度下,反应平衡时有80%的氢气变成水,且c(CO2)×c(H2)=c(CO)×c(H2O),则原混合气体中CO2和H2分子数之比是:
CO(g)+H2O(g)在一定温度下,反应平衡时有80%的氢气变成水,且c(CO2)×c(H2)=c(CO)×c(H2O),则原混合气体中CO2和H2分子数之比是:
 N2O4(g);△H<0;若初始温度相同,分别将等量的NO2气体置于编号为a、b、c的三个体积相同的密闭容器中,且已知a容器绝热恒容、b容器恒温恒容、c容器恒温恒压,则达到平衡后有关三个容器中气体颜色深浅的叙述中正确的是:
N2O4(g);△H<0;若初始温度相同,分别将等量的NO2气体置于编号为a、b、c的三个体积相同的密闭容器中,且已知a容器绝热恒容、b容器恒温恒容、c容器恒温恒压,则达到平衡后有关三个容器中气体颜色深浅的叙述中正确的是: