0 37295 37303 37309 37313 37319 37321 37325 37331 37333 37339 37345 37349 37351 37355 37361 37363 37369 37373 37375 37379 37381 37385 37387 37389 37390 37391 37393 37394 37395 37397 37399 37403 37405 37409 37411 37415 37421 37423 37429 37433 37435 37439 37445 37451 37453 37459 37463 37465 37471 37475 37481 37489 447348
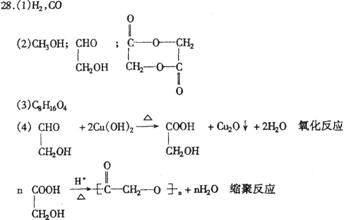
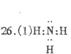

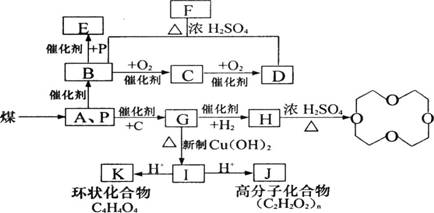
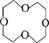

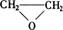 (3)已知环氧乙烷(
的结构可简写为 ,则
的分子式是
。
(3)已知环氧乙烷(
的结构可简写为 ,则
的分子式是
。
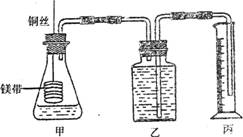
 (10分)m,n,x,y四种主族元素在周期表里的相对位置如图所示,
(10分)m,n,x,y四种主族元素在周期表里的相对位置如图所示, ?2R(g);ΔH=-QKJ/mol,平衡后,测得X和Y的转化率分别为a%和b%,已知a<b,则n值为
?2R(g);ΔH=-QKJ/mol,平衡后,测得X和Y的转化率分别为a%和b%,已知a<b,则n值为