14.下列A-D 4组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是( )
|
|
Ⅰ |
Ⅱ |
|
A |
少量SO2通入Ba(OH)2溶液中 |
过量SO2通入少量Ba(OH)2溶液中 |
|
B |
少量浓氨水滴入Al2(SO4)3溶液中 |
少量Al2(SO4)3溶液滴入浓氨水中 |
|
C |
0.1 mol Cl2通入含0.2 mol FeBr2的溶液中 |
0.3 mol Cl2通入含0.2 mol FeBr2的溶液中 |
|
D |
过量稀硝酸与少量铁屑混合 |
少量稀硝酸与过量铁屑混合 |
解析:选B。A项SO2少量生成正盐,过量生成酸式盐;B项均生成Al(OH)3;C项Ⅰ中反应为2Fe2++Cl2===2Fe3++2Cl-,Ⅱ中为2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-;D项铁屑少量生成Fe3+,铁屑过量生成Fe2+。
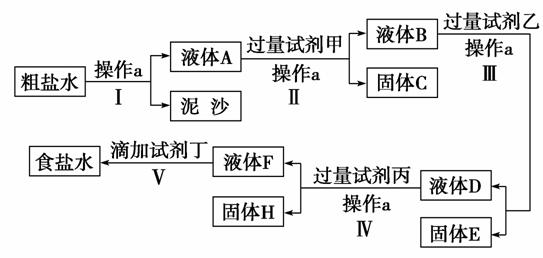
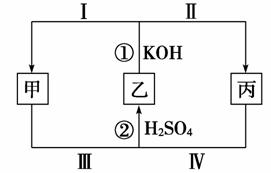 (3)H++OH-===H2O、H++CO32-===HCO3-、HCO3-+H+===H2O+CO2↑
(3)H++OH-===H2O、H++CO32-===HCO3-、HCO3-+H+===H2O+CO2↑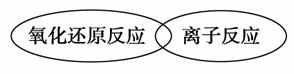 (意思正确、能表示二者的交叉关系即可)
(意思正确、能表示二者的交叉关系即可)