17.(12分)(2009年高考安徽卷)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计] 控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验。
(1)请完成以下实验设计表(表中不要留空格)。
|
实验编号 |
实验目的 |
T/K |
pH |
c/10-3mol·L-1 |
|
|
H2O2 |
Fe2+ |
||||
|
① |
为以下实验作参照 |
298 |
3 |
6.0 |
0.30 |
|
② |
探究温度对降解反应速率的影响 |
|
|
|
|
|
③ |
|
298 |
10 |
6.0 |
0.30 |
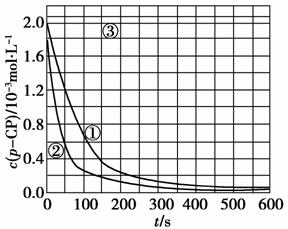
[数据处理] 实验测得p-CP的浓度随时间变化的关系如上图。
(2)请根据上图实验①曲线,计算降解反应50-150 s内的反应速率:
v(p-CP)=________mol·L-1·s-1。
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:___________________________________________________。
(4)实验③得出的结论是:pH等于10时,__________________________________________________________。
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:___________________________________________________________。
解析:本题为实验探究题,充分体现新课标精神,有一定难度。
(1)依题意可知②的实验温度为313 K,实验对比是建立在其它条件相同前提下,故pH应与①的相同。若改变pH,其它条件不变可探究溶液pH对反应速率的影响。
(2)实验①曲线中,50-150 s时:
Δc(p-CP)=1.2×10-3 mol·L-1-0.4×10-3 mol·L-1=0.8×10-3 mol·L-1,所以v(p-CP)==8.0×10-6 mol·L-1·s-1。
(3)在降解反应中,H2O2新产生的自由基起氧化作用,温度过高,H2O2因热稳定性差而分解,导致降解反应速率下降。
(4)由曲线③可知,pH=10时,c(p-CP)基本不变,反应趋于停止。
(5)由(4)得到启示:在pH=10溶液中,反应速率趋于零,可将所取样加入NaOH溶液中(使pH=10);化学反应速率随温度降低而降低,故亦可用迅速大幅降温法。
答案:(1)
|
实验 编号 |
实验目的 |
T/K |
pH |
c/10-3mol·L-1 |
|
|
H2O2 |
Fe2+ |
||||
|
① |
|
|
|
|
|
|
② |
|
313 |
3 |
6.0 |
0.30 |
|
③ |
探究溶液的pH对降解反应速率的影响 |
|
|
|
|
(2)8.0×10-6
(3)过氧化氢在温度过高时迅速分解
(4)反应速率趋向于零(或该降解反应趋于停止)
(5)将所取样品迅速加入到一定量的NaOH溶液中,使pH约为10(或将所取样品骤冷等其他合理答案均可)
 2NO2(g)(正反应吸热)。平衡后,在25 ℃时测得混合气体(N2O4和NO2)的压强为同温下N2O4(g)尚未分解时压强的1.2倍。
2NO2(g)(正反应吸热)。平衡后,在25 ℃时测得混合气体(N2O4和NO2)的压强为同温下N2O4(g)尚未分解时压强的1.2倍。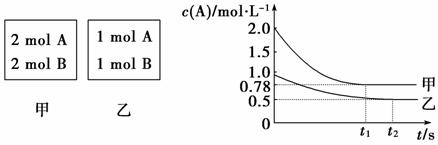
 600 ℃时,在一密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g)
600 ℃时,在一密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g) 2H2O(g) K2=2×1081
2H2O(g) K2=2×1081