1.(上海高考题)过氧化氢的沸点比水高,但受热容易分解。某试剂厂先制得7%~8%的过氧化氢溶液,再浓缩成30%溶液时,可采用的适宜方法是
A.常压蒸馏 B.减压蒸馏
C.加生石灰常压蒸馏 D.加压蒸馏
9.密闭容器中X、Y、Z三种气体的初始浓度和不同温度下的平衡浓度如下表:
|
物质 |
X |
Y |
Z |
|
25℃时初始浓度/mol/L |
0.1 |
0.2 |
0 |
|
25℃时平衡浓度/mol/L |
0.05 |
0.05 |
0.1 |
|
50℃时平衡浓度/mol/L |
0.06 |
0.08 |
0.08 |
下列说法错误的是
A.该反应是放热反应
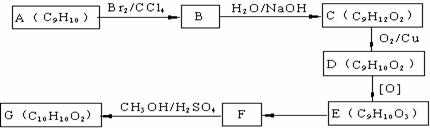
B.该反应可表示为 X(g)+3Y(g) 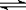 2Z(g)
2Z(g)
C.平衡后若增大压强,原平衡将向生成Z的方向移动,X浓度将比原来减少
D.反应达到平衡时,Y的分解速率是Z的分解速率的1.5倍
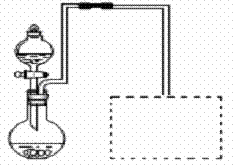
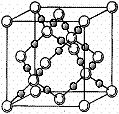 ;与该最简单分子互为等电子体的阳离子为 。
;与该最简单分子互为等电子体的阳离子为 。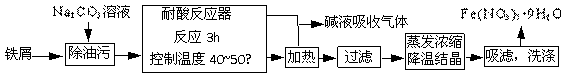

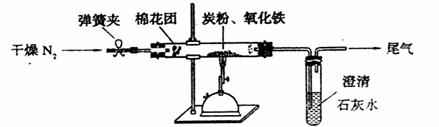 ⑵设计方案 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比
⑵设计方案 如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比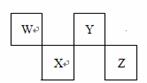 (15分)W、X、Y、Z四种短周期元素在元素周期表中
(15分)W、X、Y、Z四种短周期元素在元素周期表中 的位置如右图所示,其中
的位置如右图所示,其中 (2)H2Y2的电子式为 ,Na2Y2中
(2)H2Y2的电子式为 ,Na2Y2中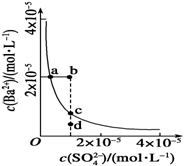 某温度时,BaSO4在水中的沉淀溶解平衡曲线如右图所示。
某温度时,BaSO4在水中的沉淀溶解平衡曲线如右图所示。