9.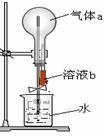 如右图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成喷泉的组合是
如右图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成喷泉的组合是
|
|
干燥气体a |
液体b |
|
A |
NH3 |
水 |
|
B |
Cl2 |
饱和食盐水 |
|
C |
HCl |
水 |
|
D |
CO2 |
NaHCO3溶液 |
9. 如右图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成喷泉的组合是
如右图所示,在干燥的圆底烧瓶中充满某气体a,胶头滴管中吸有少量液体b,当把溶液b挤进烧瓶后,打开止水夹不能形成喷泉的组合是
|
|
干燥气体a |
液体b |
|
A |
NH3 |
水 |
|
B |
Cl2 |
饱和食盐水 |
|
C |
HCl |
水 |
|
D |
CO2 |
NaHCO3溶液 |