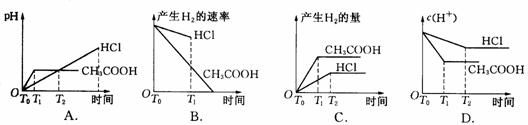
26.10℃时,在烧杯中加入0.1mol/L的 NaHCO3溶液400mL,加热,测得该溶液的pH发生如下变化:
|
温度(℃) |
10 |
20 |
30 |
50 |
70 |
|
pH |
8.3 |
8.4 |
8.5 |
8.9 |
9.4 |
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为 。
(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度_______(填“大于”或“小于”)NaHCO3 。

 (3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液的pH,若pH8.3_______(填“>”、“<”或“=”),说明甲正确,若pH 8.3(填“>”、“<”或“=”),说明乙正确。
(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液的pH,若pH8.3_______(填“>”、“<”或“=”),说明甲正确,若pH 8.3(填“>”、“<”或“=”),说明乙正确。
(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:
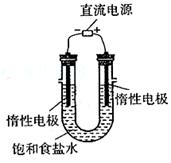
实验装置如右图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明 (填“甲”或“乙”)推测正确。
(5)资料:将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1。据此资料可以判断 (填“甲”或“乙”)推测正确,原因是 。
23.下图是Zn和Cu形成的原电池,某实验兴趣小组做完试验后,在读书卡片上记录如下:
|
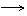

(1)在卡片上,描述合理的是 ( )
A.①②③ B. ④⑤⑥ C. ②③④ D. ③④⑤
(2)该原电池的总反应方程式 ,你所知道的构成原电池的条件是 ;
(3)生活中因为原电池反应而使得金属发生最常见的 这种电化学腐蚀,请列举两种方法来防止金属的电化学腐蚀 、
20、现有常温下的四种溶液(如下表),下列有关叙述中正确的是( )
|
|
① |
② |
③ |
④ |
|
溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
|
pH |
11 |
11 |
3 |
3 |
A.在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变
B.温度下降10℃,四种溶液的pH均不变
C.分别加水稀释10倍、四种溶液的pH:①>②>④>③
D.将①、④两种溶液等体积混合,所得溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
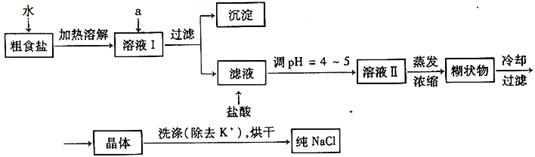
 (2)用提纯的NaCl配制500mL4.00 mol·L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有_____________(填仪器名称)。
(2)用提纯的NaCl配制500mL4.00 mol·L-1NaCl溶液,所用仪器除药匙、玻璃棒外还有_____________(填仪器名称)。 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
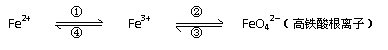
 NaHCO3↓+NH4Cl ①
NaHCO3↓+NH4Cl ① 
 CaO+CO2↑②
CaO+CO2↑②
 2NH3
③
2NH3
③ 

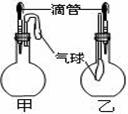 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响)。则所用试剂分别可能依次是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响)。则所用试剂分别可能依次是( )