20、(深圳市宝安区一模)(11分)铝及铝合金经过阳极氧化,铝表面能生成几十微米的较厚的氧化铝膜。
Ⅰ、某研究性学习小组模拟工业法对铝片表面进行氧化处理。他们的实验步骤如下:
a.铝片的预处理,取出一定大小的铝片,依次用苯、酒精擦洗铝片的表面
 b.用水冲洗经有机物擦洗的铝片,浸入60-70℃的2mol/L的NaOH溶液中,以除去原有的氧化膜,约l min后,取出用水冲洗干净,再用钼酸铵溶液处理以抑制电解生成的氧化铝被硫酸溶解。
b.用水冲洗经有机物擦洗的铝片,浸入60-70℃的2mol/L的NaOH溶液中,以除去原有的氧化膜,约l min后,取出用水冲洗干净,再用钼酸铵溶液处理以抑制电解生成的氧化铝被硫酸溶解。
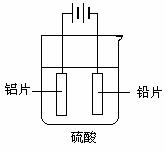
c.阳极氧化。以铅为阴极,铝片为阳极,以硫酸溶液为电解液,按照如图连接电解装置,电解40min后取出铝片,用水冲洗,放在水蒸汽中封闭处理20-30min,即可得到更加致密的氧化膜。
试回答下列问题
(1)用苯和酒精擦拭铝片的目的: ,
氢氧化钠溶液处理铝片时反应的离子方程式是:
。
(2)阳极的电极反应式为: 。
(3)下列有关说法正确的是 (填序号)。
A.电解时电子从电源负极→导线→铅极,铝极→导线→电源正极
B.在电解过程中,H+ 向阳极移动,SO42-向阴极移动
C.电解过程中溶液的PH基本不变
D.电解时,铝片为阳极,被氧化
Ⅱ、另一小组针对铝表面保护膜的保护作用展开了研究,他们查阅有关资料得知:尽管铝表面致密的氧化膜能使铝与其周围的介质(空气、水等)隔绝,对铝制品起到保护作用,但铝制容器仍不能长期用来盛放和腌制咸菜。究其原因,该小组设计了一个实验以探究其中的原因。他们的实验过程如下:
|
实验 编号 |
实验过程 |
实验现象 |
|
1 |
取一小片铝片于试管中,加入1.0 mol·L-1的盐酸2ml |
30秒时开始有少量气泡,然后产生气泡的速率加快,最后铝片消失。 |
|
2 |
取一小片铝片于试管中,加入0.5mol·L-1的硫酸2ml |
55秒时开始有少量气泡,然后产生气泡速率加快,最后片铝消失。 |
|
3 |
取一小片铝片于试管中,加入氯化铜稀溶液 |
3分钟左右表面产生少量气泡,且铝表面析出一些红色固体。 |
|
4 |
取一小片铝片于试管中,加入硫酸铜稀溶液 |
一直没有明显的变化 |
你认为实验1、2中盐酸和硫酸的浓度分别为1.0 mol·L-1、0.5mol·L-1的原因是
根据该实验现象,你认为铝制容器不能长期盛放和腌制咸菜的原因是
。
23.(广东佛山市南海区调研)实验探究题(18分)
Ⅰ.某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入1-2滴溴水,振荡后溶液呈黄色。
(1)提出问题: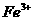 、
、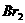 谁的氧化性更强?
谁的氧化性更强?
(2)猜想:
①甲同学认为氧化性: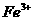 >
>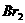 ,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含_▲_(填化学式,下同)所致。
,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含_▲_(填化学式,下同)所致。
②乙同学认为氧化性: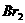 >
> 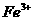 ,故上述实验现象是发生化学反应所致,则溶液呈黄色是含_▲_所致。
,故上述实验现象是发生化学反应所致,则溶液呈黄色是含_▲_所致。
(3)设计实验并验证:
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a. 酚酞试液 b. 四氯化碳 c. 无水酒精 d. 硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
|
|
选用试剂 |
实验现象 |
|
方案1 |
|
|
|
方案2 |
|
|
(4)应用与拓展:
①在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为_▲_。
②在100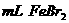 溶液中通入
溶液中通入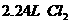 (标准状况),溶液中有1/3的Br-被氧化成单质
(标准状况),溶液中有1/3的Br-被氧化成单质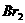 ,则原
,则原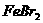 溶液中
溶液中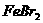 的物质的量浓度为_▲_。
的物质的量浓度为_▲_。
 2ZnO+2SO2 2C+O2
2ZnO+2SO2 2C+O2
 (2)因氢气易燃易爆,贮运安全极为重要。已知氢气的燃烧热为285.8kJ·mol-1。写出其完全燃烧的热化学方程式: 。
(2)因氢气易燃易爆,贮运安全极为重要。已知氢气的燃烧热为285.8kJ·mol-1。写出其完全燃烧的热化学方程式: 。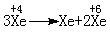 。XeF6则发生非氧化还原反应完全水解(已知:
。XeF6则发生非氧化还原反应完全水解(已知: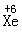 在水中主要以XeO3分子形式存在)。试回答下列问题:
在水中主要以XeO3分子形式存在)。试回答下列问题: 在常温或不太高的温度下,可将氟盛装在铜、铁、镁、镍(或其它的合金)制成的容器中,原因是_____________________________________________________。
在常温或不太高的温度下,可将氟盛装在铜、铁、镁、镍(或其它的合金)制成的容器中,原因是_____________________________________________________。 ),溶液的c(H+)为_____,c(F-)为_____。
),溶液的c(H+)为_____,c(F-)为_____。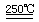 HgO+CaBr2(1分) 循环过程需要很高的能量,且使用重金属汞,会产生污染。(2分) (3)①:SO2+O2+2H2O
HgO+CaBr2(1分) 循环过程需要很高的能量,且使用重金属汞,会产生污染。(2分) (3)①:SO2+O2+2H2O 2HI+H2SO4(1分) ②:2H2SO4
2HI+H2SO4(1分) ②:2H2SO4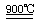 2SO2↑+O2↑+2H2O (1分) SO2和I2
可循环使用,无污染。(1分) (4)①<(1分) ②:加快;增大(2分) ③:Cu2O+CO
2SO2↑+O2↑+2H2O (1分) SO2和I2
可循环使用,无污染。(1分) (4)①<(1分) ②:加快;增大(2分) ③:Cu2O+CO Cu+CO2
(2分 不写可逆号扣1分)
Cu+CO2
(2分 不写可逆号扣1分)