18.(广东卷21).(12分)
某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由 。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1H2SO4/3% H2O2、6 mol·L-1HNO3/0.01 mol·L-1KmnO4、NaOH稀溶液、0.1 mol·L-1Kl、20% KSCN、蒸馏水。
① 提出合理假设
假设1: ;
假设2: ;
假设3: 。
② 设计实验方案证明你的假设(不要在答题卡上作答)
③ 实验过程
根据②的实验方案,进行实验。请在答题卡上按下表格式写出实验操作步骤、预期现象与结论。
|
实验操作 |
预期现象与结论 |
|
步骤1: |
|
|
步骤2: |
|
|
步骤3: |
|
|
… |
|
解析:。(1) 该结论不正确。稀HNO3有强氧化性,若该铁的价态为+2价,则被氧化为+3价同样可使KSCN溶液变血红色。
(2) ①提出合理假设
假设1:催化剂中铁元素的价态为+3价。
假设2:催化剂中铁元素的价态为+2价。
假设3:催化剂中铁元素的价态既有+3价也有+2价。
②设计实验方法证明你的假设
③实验过程
|
实验操作 |
预期现象与结论 |
|
步骤1:将适量稀H2SO4加入少许样品于试管中,加热溶解; |
溶液呈黄绿色,说明溶液中含Fe2+或Fe3+。 |
|
步骤2:取少量溶液,滴加酸性KMnO4溶液。 |
若KMnO4溶液的紫红色褪去为无色溶液,则说明催化剂中铁元素的价态含+2价;若不褪色,则说明催化剂中铁元素的价态不含+2价。 |
|
步骤3:另取少量溶液,滴加KSCN溶液。 |
若溶液变为血红色,则说明催化剂中铁元素的价态含+3价;若溶液无明显变化,则说明催化剂中铁元素的价态不含+3价。 |
17.(广东卷20).(11分)
某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
|
实验编号 |
T/K |
大理石规格 |
HNO3浓度/mol·L-1 |
实验目的 |
|
① |
298 |
粗颗粒 |
2.00 |
(Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响;) |
|
② |
|
|
|
|
|
③ |
|
|
|
|
|
④ |
|
|
|
(2)实验①中CO2质量随时间变化的关系见下图:
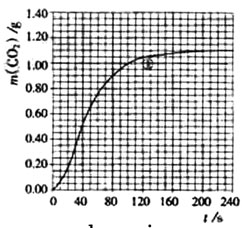 依据反应方程式
依据反应方程式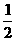 CaCO3+HNO3=
CaCO3+HNO3=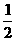 Ca(NO3)2+
Ca(NO3)2+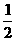 CO2↑+
CO2↑+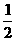 H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程)。
H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程)。
(3)请在答题卡的框图中,画出实验②、③和④中CO2质量随时间变化关系的预期结果示意图。
解析:
|
实验编号 |
T/K |
大理石规格 |
HNO3浓度/mol·L-1 |
实验目的 |
|
① |
298 |
粗颗粒 |
2.00 |
⑴实验①和②探究HNO3浓度对该反应速率的影响; ⑵实验①和③探究温度对该反应速率的影响。 ⑶实验①和④探究大理石规格(粗、细)对该反应的影响。 |
|
② |
298 |
粗颗粒 |
1.00 |
|
|
③ |
308 |
粗颗粒 |
2.00 |
|
|
④ |
298 |
细颗粒 |
2.00 |
(2)
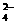 等杂质,提纯工艺路线如下:
等杂质,提纯工艺路线如下: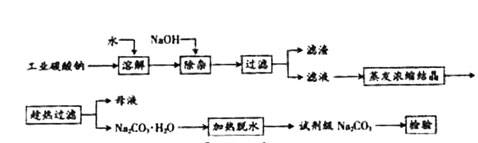
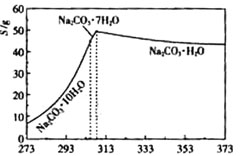 已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
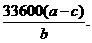 (6)偏小.
(6)偏小.
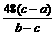
 [知识点归纳]
[知识点归纳]