10.(16分)二氧化钛是一种不溶于稀酸的物质,常用于制取金
属钛。某种金红石矿石的主要成分是TiO2,含有Fe2O3和Al2O3杂质。一研究性学习小组设计如下方案制备金属钛,并得到其它副产品。
(1)已知Fe(OH)3、Al(OH)3,开始沉淀的pH数据(见下表)
|
氢氧化物 |
Fe(OH)3 |
A1(OH)3 |
|
开始沉淀pH |
1.5 |
3.3 |
向溶液I中滴加NaOH溶液,并调溶液pH,若开始只得到一种沉淀,该沉淀是
,应控制pH的范围是 ,反应的离子方程式是 ;
(2)向溶液Ⅱ中“继续加适量NaOH溶液”,若操作不当会减少滤渣Ⅲ的质量,请你设计另一种方案代替向溶液Ⅱ中“继续加适量NaOH溶液”的方案,该方案是 ,反应的离子方程式是 ;
(3)已知:①CO2(g)==C(s)+O2(g); △H=393.5 kJ·mol-l
②CO(g)+ O2(g)==CO2(g); △H=-283 kJ·mol-l
③TiO2(s)+2Cl2(g)==TiCl4(s)+O2(g);△H =141 kJ·mol-l
写出TiO2与Cl2+C反应的热化学方程式 。
(4)若经过多步反应后制得b g金属钛,则金红石矿石中TiO2的质量分数为
 (3)为了验证CH4是否具有还原性,某小组设计了如下实验:
(3)为了验证CH4是否具有还原性,某小组设计了如下实验: 之间发生怎样的反应。可能发生的反应有:2Fe3++SO
之间发生怎样的反应。可能发生的反应有:2Fe3++SO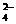 +2H+(氧化还原反应)
+2H+(氧化还原反应)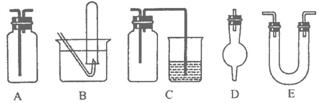 (14分)下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。
(14分)下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。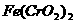 和
和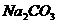 固体混合物;
固体混合物;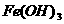 胶体;
胶体; 饱和溶液时,加入少量的稀硫酸.
饱和溶液时,加入少量的稀硫酸. (5)为比较Fe3+和Cu2+对H2O2分解的催化效果,某同学设计了下图所示的实验。
(5)为比较Fe3+和Cu2+对H2O2分解的催化效果,某同学设计了下图所示的实验。
 (12分)氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂。实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵:
(12分)氟化钠是一种重要的氟盐,主要用作农业杀菌剂、杀虫剂、木材防腐剂。实验室可通过下图所示的流程以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵: (10分)某兴趣小组同学共同设计了如图所示的实验装置。该装置既可用于制取气体,又可用于验证物质的性质。
(10分)某兴趣小组同学共同设计了如图所示的实验装置。该装置既可用于制取气体,又可用于验证物质的性质。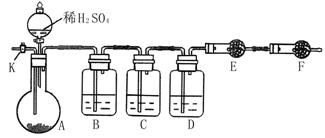
 ZnSO4+SO2↑+2H2O计算后,取65.0 g锌粒与98%的浓硫酸(ρ=1.84 g/cm3)110mL充分反应,待锌粒全部溶解后,收集所得气体X。经测定其中含有气体杂质。
ZnSO4+SO2↑+2H2O计算后,取65.0 g锌粒与98%的浓硫酸(ρ=1.84 g/cm3)110mL充分反应,待锌粒全部溶解后,收集所得气体X。经测定其中含有气体杂质。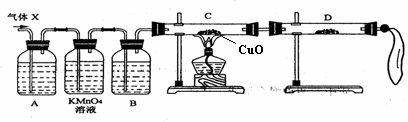 (2)为了检验主要杂质气体的成分,化学兴趣小组的同学设计了如下实验,对气体(X)取样进行认真探究。
(2)为了检验主要杂质气体的成分,化学兴趣小组的同学设计了如下实验,对气体(X)取样进行认真探究。 (3)将硫酸亚铁溶液与硫酸铵溶液混合,结晶得摩尔盐。
(3)将硫酸亚铁溶液与硫酸铵溶液混合,结晶得摩尔盐。