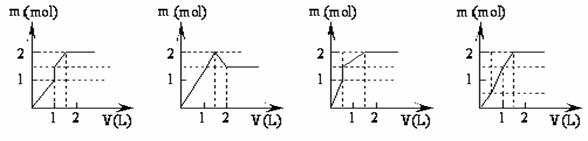
10.(14分)(原创)在食品加工领域,应用二氧化硫的最主要原因是避免氧化和防腐。在我国葡萄酒中二氧化硫的最大使用量为0.2500g/kg,二氧化硫残留量不得超过0.05000g/kg。葡萄酒中的二氧化硫包括游离的和结合的,因而加人氢氧化钾使之破坏其结合状态,并使之固定S02+2KOH == K2S03+H20;然后加入硫酸又使二氧化硫游离,K2S03+H2S04 == K2S04+H2O+S02↑;加入过量的I2氧化S02;过量的I2可用硫代硫酸钠进行滴定,I2+2Na2S203== Na2S406+ 2NaI。
以下是某实验小组测定某品牌的干白葡萄酒(密度为1.12g/ml)中二氧化硫的含量是否超标的实验方案。
实验步骤:
①用移液管量取50.00ml样品于250ml锥形瓶中,加入25.00 ml1mol/L氢氧化钾溶液,加塞,摇匀;ww.k@s@5@ 高#考#资#源#网
②静置15min;
③打开塞子,加入25.00ml1:3硫酸溶液使溶液呈酸性,再加入25.00ml0.01000mol/L碘溶液,迅速的加塞,摇匀;
④用 滴定管移取步骤③中溶液25.00ml,加入适量0.1%的A溶液作指示剂,立即用浓度为0.002000mol/L的硫代硫酸钠溶液滴定,并记录消耗硫代硫酸钠溶液的体积;
⑤重复以上实验2次;
⑥数据处理,得出结论。
请回答下列问题:
(1)以上实验方案中步骤③中加碘溶液时发生的离子反应方程式是: ;
(2)步骤①-③中始终要将锥形瓶加塞进行操作的原因是 ;
(3)步骤④的A溶液最合适的是 ;滴定终点的判断方法是 ;
(4)步骤④应该选用 (填空“酸式”或“碱式”)滴定管;
(5)该小组三次实验消耗的Na2S203溶液的体积数据记录如下:
|
序号 |
滴定前/mL |
滴定后/mL |
|
① |
1.35 |
19.40 |
|
② |
1.05 |
19.00 |
|
③ |
1.58 |
20.91 |
根据数据计算该样品中总二氧化硫的浓度为 mol/L,故该干白葡萄酒是 (填“合格”“不合格”)产品。
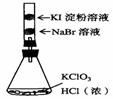
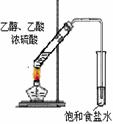
5. (原创)实验室里运用下列实验装置进行实验,能达到相应实验目的并符合环保的是
|
A |
B |
C |
D |
 |
 |
 |
 |
|
完成氯气的性质实验 |
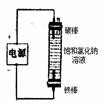
制取84消毒液(NaClO) |
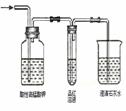
检验二氧化硫中是否混有二氧化碳 |
制取乙酸乙酯 |
3. (原创)下列热化学方程式或离子方程式中,正确的是
A.碳酸钠溶液中滴加少量的硫酸氢钠溶液:CO32- + H+ == HCO3-
|

 N2(g) + 3H2(g)
2NH3(g)
△H=-38.6kJ·mol-1ww.k@s@5@
高#考#资#源#网
N2(g) + 3H2(g)
2NH3(g)
△H=-38.6kJ·mol-1ww.k@s@5@
高#考#资#源#网
C.醋酸铵溶液中的水解离子方程式:C H3COO- + H2O  C H3COO H+ OH-
C H3COO H+ OH-
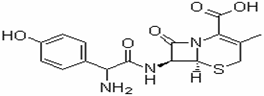
D. 尼泊金酸(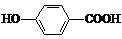 )与碳酸氢钠溶液反应:
)与碳酸氢钠溶液反应:
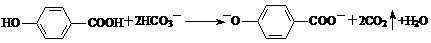
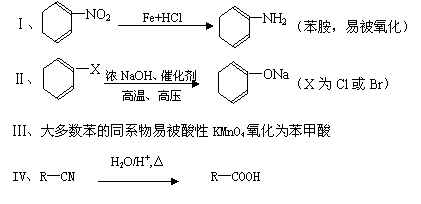 已知:
已知: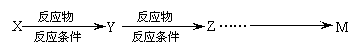
 CO(g)+H2(g);ΔH=
。(用含ΔH1、ΔH2的代数式表示)
CO(g)+H2(g);ΔH=
。(用含ΔH1、ΔH2的代数式表示)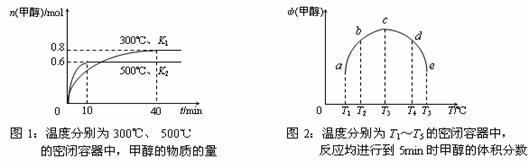
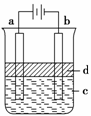 (2)利用电解实验可以制得纯净的Fe(OH)2白色沉淀,如图所示,已知两电极的材料分别为石墨和铁。
(2)利用电解实验可以制得纯净的Fe(OH)2白色沉淀,如图所示,已知两电极的材料分别为石墨和铁。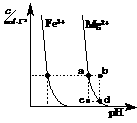 (3)右图为某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度变化情况。据图分析:
(3)右图为某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度变化情况。据图分析: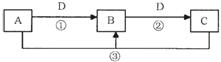
 ·H2O
·H2O