19.(10分)下面是元素周期表的一部分,表中所列字母分别代表某一化学元素。
|
a |
|
b |
|||||||||||||||
|
|
|
|
|
|
c |
d |
|
|
|||||||||
|
e |
|
f |
|
|
|
g |
h |
||||||||||
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
j |
(1)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图____。
(2)NH3·H2O的电离方程式NH3·H2O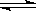 NH4++OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构_________(填字母代号)。
NH4++OH-,试判断NH3溶于水后,形成的NH3·H2O的合理结构_________(填字母代号)。
(a)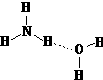 (b)
(b)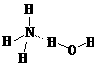
(3)上表中的c原子间也可形成链状结构,假设c原子间只以单键形式连接,并形成与直链烷烃类似的氢化物,则该系列氢化物的通式为___________________。
(4)利用稀有气体化合物,人们实现了许多制备实验上的突破。如用j的+6价氧化物在碱性条件下与NaBrO3反应生成NaBrO4, 同时生成j的单质。写出上述反应的方程式_____
_______。
同时生成j的单质。写出上述反应的方程式_____
_______。
(5)、若已知原子结构规律不变,则第166号新元素在元素周期表中位置: 。
[答案]
(1)+26 2 8 14 2
(2)b
(3)NnHn+2
(4)3NaBrO3+XeO3=3NaBrO4+Xe
(5)、八VIA
17.(10分)在一定温度下的某容积可变的密闭容器中,建立下列化学平衡:
C(s)+H2O(g)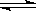 CO(g)+H2(g)
CO(g)+H2(g)
试分析和回答下列问题:
(1)可认定上述可逆反应在一定条件下已达到化学平衡状态的是 (选填序号)。
A 体系的压强不再发生变化 B v正(CO)=v逆(H2O)
C 生成n molCO的同时生成n mol H2 D 1mol H-H键断裂的同时断裂2mol H-O键
(2)若上述化学平衡状态从 正反应开始建立,达到平衡后,给平衡体系加压(缩小容积、其它条件不变。下同),则容器内气体的平均相对分子质量面将 (填写不变、变小、变大)。
正反应开始建立,达到平衡后,给平衡体系加压(缩小容积、其它条件不变。下同),则容器内气体的平均相对分子质量面将 (填写不变、变小、变大)。
(3)若上述化学平衡状态从正、逆两反应同时建立[即起始时同时投放C(s)、H2O(g)、CO(g)、H2(g)],达到平衡后,试讨论:
①容积内气体混合物的平均相对分子质量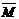 的取值范围是
。
的取值范围是
。
②若给平衡体系加压,请参照起始投放的气体物质的平均相对分子质量(设定为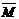 1),分别给出
1),分别给出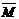 的变化:(填“增大”、“减小”、“不变”)
的变化:(填“增大”、“减小”、“不变”)
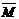 1的取值 1的取值 |
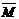 的变化 的变化 |
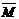 1<12 1<12 |
|
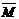 1=12 1=12 |
不变 |
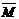 1>12 1>12 |
|
[答案](1)B、D
(2)变大
(3)①2<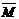 <28
②若
<28
②若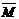 1<12,则
1<12,则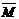 变小;;
变小;;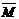 1>12则
1>12则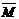 变大。
变大。
13.
|
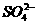 的物质的量浓度为6mol·L-1,则此溶液最多溶解铁粉的质量为( )
的物质的量浓度为6mol·L-1,则此溶液最多溶解铁粉的质量为( )
A.5.6 g B.11.2g C.22.4g D.33.6g [答案]C
14下列物质中,既能与NaOH溶液反应,又能与HNO3反应,还能水解的是
①Al2O3 ②H2S ③NaHS ④氨基酸 ⑤对-羟基苯甲酸钠 ⑥乙醇 ⑦纤维素 ⑧蛋白质
A ③④⑤⑥⑦⑧ B ③⑤⑧ C ③⑤⑥⑦⑧ D 全部 [答案]B
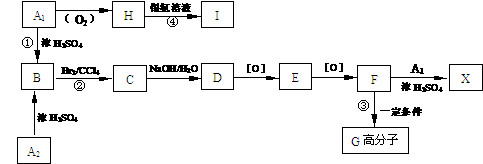
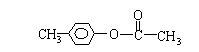
 (3)
(3)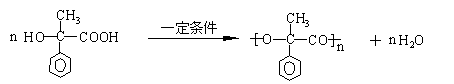
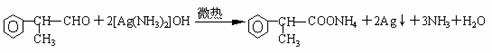 (4)
(4)
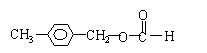
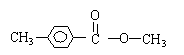
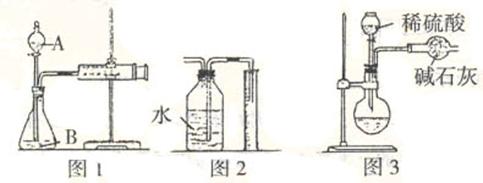
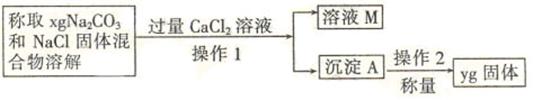
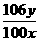
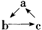 的转化关系。(“→”表示在一定条件下可
的转化关系。(“→”表示在一定条件下可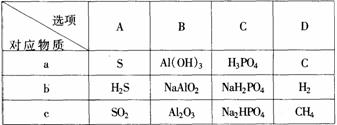
 A.产生气体体积 ①=②
A.产生气体体积 ①=②