0 23407 23415 23421 23425 23431 23433 23437 23443 23445 23451 23457 23461 23463 23467 23473 23475 23481 23485 23487 23491 23493 23497 23499 23501 23502 23503 23505 23506 23507 23509 23511 23515 23517 23521 23523 23527 23533 23535 23541 23545 23547 23551 23557 23563 23565 23571 23575 23577 23583 23587 23593 23601 447348
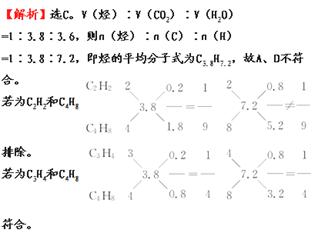
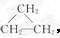 后者为CH2==CH2,
后者为CH2==CH2, 

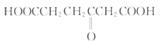

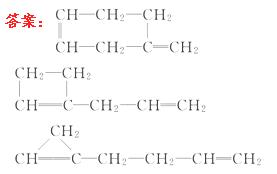
 O的原子个数之比,能否求出该酯的分子式? _____(填“能”或“不能”),原因是___
O的原子个数之比,能否求出该酯的分子式? _____(填“能”或“不能”),原因是___ 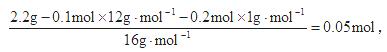
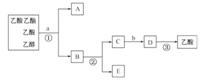
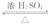 CH3COOC2H5+H2O
CH3COOC2H5+H2O
 (2)若用图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为___________、___________等。
(2)若用图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为___________、___________等。 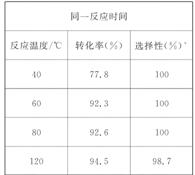

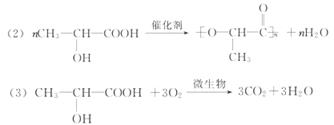
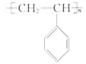 )材料所带来的白色污染问题甚为突
)材料所带来的白色污染问题甚为突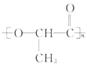 包装材料。
包装材料。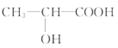 )可以从甜菜发酵的糖
)可以从甜菜发酵的糖