8.为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是
|
|
被提纯的物质 |
除杂试剂 |
分离方法 |
|
A |
溴化钠溶液(NaI) |
氯水、 |
萃取、分液 |
|
B |
苯(苯酚) |
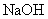 溶液 溶液 |
过滤 |
|
C |
 |
饱和 溶液 溶液 |
洗气 |
|
D |
乙醇(乙酸) |
新制生石灰( ) ) |
蒸馏 |
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较用下图装置进行实验,实验时均以生成 气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:
气体为准,其它可能影响实验的因素均已忽略,相关数据见下表:

|
实验序号 |
 质量 质量 |
其它物质质量 |
待测数据 |
|
④ |
 |
无其他物质 |
|
|
⑤ |
 |
  |
|
|
⑥ |
 |
  |
|
回答下列问题:
(4)上述实验中的“待测数据”指 ;
(5)本实验装置图中量气装置B由干燥管、乳胶管和 滴定管改造后组装而成,此处所用滴定管是
(填“酸式”或“碱式”)滴定管;
滴定管改造后组装而成,此处所用滴定管是
(填“酸式”或“碱式”)滴定管;
(6)若要证明实验⑤中干燥管内收集的气体是 ,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
;
,可待气体收集结束后,用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,
;
(7)若 氯酸钾完全分解,则在标准状况下可得氧气多少
氯酸钾完全分解,则在标准状况下可得氧气多少  。
。
28.(12分)在某个容积为 的密闭容器内,在T℃时按下图1所示发生反应:
的密闭容器内,在T℃时按下图1所示发生反应:


 ,
, (
( 、
、 、
、 、
、 为最简整数比)。
为最简整数比)。

(1)据图l所示,反应开始至达到平衡时,用D表示该反应速率为 ;
(2)该反应的化学平衡常数K的数值为 (保留至两位小数);
(3)反应达到平衡后,第7min时:
①若降低温度,D的浓度变化最可能的是 (用图2中a-c的编号回答):
②若在7min时仍为原平衡,此时将容器的容积压缩为原来一半,请在图3中画出7min后D浓度变化情况。
(4)在T℃时,相同的容积为 的密闭容器内,若开始时加入
的密闭容器内,若开始时加入 、
、 、
、 、
、 反应,达到平衡后,A的浓度范围为
。
反应,达到平衡后,A的浓度范围为
。
(5)下面四个选项是四位学生在学习化学反应速率与化学反应限度以后,联系化工生产实际所发表的看法,你认为不正确的是 。
A.利用化学反应速率理论可指导怎样在一定时间内快出产品
B.加快反应速率可提高原料的转化率
C.勒夏特列原理可指导怎样使用有限原料多出产品
D.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
29.(16分)我国目前的身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式为:

已知:
(1)

(2) (
( 、
、 、
、 表示烃基)这种材料可采用下合成路线:
表示烃基)这种材料可采用下合成路线:

试回答下列问题:
(1)反应②⑥加入的试剂X是
(2)①的反应类型是
(3)写出结构简式:B I
(4)合成时应控制的单体的物质的量
 : : (用m、n表示)
: : (用m、n表示)
(5)写出化学方程式:
反应③ 反应⑥:
(6)物质I的同分异构体符合下列条件
①苯环上有三个取代基且分别处于间位,其中一个是醛基
②能与 溶液发生显色反应
溶液发生显色反应
③不能与 溶液反应放出
溶液反应放出 气体,但能在
气体,但能在 溶液中发生水解反应符合以上条件的I的同分异构体有
种,写出其中任意两种的结构简式:
溶液中发生水解反应符合以上条件的I的同分异构体有
种,写出其中任意两种的结构简式:
、
27.(13分)A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+、Ag+和阴离子NO3-、OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复)。现做如下实验:
|
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀。
请回答下列问题:
(1)根据以上事实推断A-E的化学式:
A ;B ;C ;D ;E 。
(2)请用离子方程式表示A溶液显碱性的原因 。
(3)写出②、③、④的离子方程式:② ;③ ;④ 。


 溶液与过量NaOH溶液反应:
溶液与过量NaOH溶液反应:
 :
:
 )含氮量很高,可作为饲料添加剂
)含氮量很高,可作为饲料添加剂 研细后倒入烧杯,加
研细后倒入烧杯,加 蒸馏水溶解;
蒸馏水溶解; 溶液中逐滴加入
溶液中逐滴加入 ,能显著提高奶粉的含氮检测量
,能显著提高奶粉的含氮检测量

 中的
中的 气体
气体 的
的
 溶液中分别加入
溶液中分别加入 冰醋酸、
冰醋酸、 、
、 固体,则溶液中
固体,则溶液中 浓度的变化依次为:( )
浓度的变化依次为:( ) 代表阿伏加德罗常数的数值,下列说法中正确的是:①常温常压下,
代表阿伏加德罗常数的数值,下列说法中正确的是:①常温常压下, 甲基
甲基 所含的中子数为
所含的中子数为 ;②常温常压下,
;②常温常压下,
 气体的分子数小于
气体的分子数小于 ;③
;③ 的铜发生氧化还原反应,一定失去
的铜发生氧化还原反应,一定失去 个电子;④常温常压下,
个电子;④常温常压下,
 的乙酸溶液中,乙酸的分子数目小于
的乙酸溶液中,乙酸的分子数目小于 ;⑤标况时,
;⑤标况时, 氦气含有的核外电子数为
氦气含有的核外电子数为





 加成
加成 。关于此电池,下列说法正确的是( )
。关于此电池,下列说法正确的是( ) 为负极,
为负极, 为正极,
为正极,
 能通过薄层纸片向附着二氧化锰的电极移动
能通过薄层纸片向附着二氧化锰的电极移动 为4的
为4的 溶液中:
溶液中:
 的溶液中:
的溶液中:
 溶液与
溶液与
 盐酸混合:
盐酸混合:
 溶液中:
溶液中:

 氢氧化钠溶液,直至形成透明溶液。请根据实验现象出现的先后顺序,依次写出离子方程式① 、② 、③ 。
氢氧化钠溶液,直至形成透明溶液。请根据实验现象出现的先后顺序,依次写出离子方程式① 、② 、③ 。
 表示不同的原子,连结表示原子间的共价键)则G的结构简式为
。
表示不同的原子,连结表示原子间的共价键)则G的结构简式为
。


