24.(6分)标准状况下进行下列实验:甲、乙、丙各取30.0mL同浓度的盐酸,加入同一种镁铝合金,所取合金质量和产生气体的体积如表所列,计算:
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量(mg) |
510 |
765 |
1530 |
|
气体体积(mL) |
560 |
672 |
672 |
(1)盐酸的物质的量浓度;
(2)合金中Mg和Al的质量之比;
(3)丙实验后,还需向容器中加入上述盐酸溶液多少mL才能使剩余固体恰好完全溶解。
23.(11分)1L某混合溶液,可能含有的离子如下表:
|
可能大量含有的阳离子 |
H+、K+、Mg2+、Al3+、NH4+、Fe2+、Fe3+ |
|
可能大量含有的阴离子 |
Cl-、Br-、I-、ClO-、AlO2- |
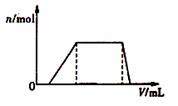
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。则该溶液中确定含有的离子是 ,一定不含的的阳离子是 ,一定不存在的阴离子是 。
(2)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
|
Cl2的体积(标准状况) |
2.8L |
5.6L |
11.2L |
|
n(Cl-) |
1.25mol |
1.5mol |
2mol |
|
n(Br-) |
1.5mol |
1.4mol |
0.9mol |
|
n(I-) |
a mol |
0 |
0 |
①当通入Cl2的体积为2.8L时,溶液中发生反应的离子方程式为 。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为 。
20.(6分)根据下表中提供的数据回答问题。
|
|
NaCl |
MgCl2 |
AlCl3 |
SiCl4 |
|
熔点 |
810℃ |
710℃ |
180℃ |
-68℃ |
|
沸点 |
1465℃ |
1418℃ |
160℃ |
57℃ |
(1)根据表中数据推测,上述四种氯化物中属于分子晶体的是 。
(2)另设计一个实验,判断氯化铝是离子化合物还是共价化合物
。
(3)NaCl的键的强度比MgCl2的 。(填“强”“弱”或“无法比较”)