21.(12分)实验室制取甲酸乙酯的反应为:
HCOOH+CH3CH2OH HCOOCH2CH3+H2O
HCOOCH2CH3+H2O
反应在该条件下进行时各物质的浓度(mol·L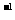 )随时间的变化如下表:
)随时间的变化如下表:
|
时间(min) |
HCOOH |
CH3CH2OH |
HCOOCH2CH3 |
H2O |
|
0 |
0.3 |
0.7 |
0 |
0.3 |
|
10 |
0.23 |
a |
b |
c |
|
20 |
0.2 |
0.6 |
0.1 |
0.4 |
有关物质在101.3KPa时沸点如下:
|
|
HCOOH |
CH3CH2OH |
HCOOCH2CH3 |
H2O |
|
沸点(℃) |
101 |
78.5 |
54 |
100 |
(1)写出该反应的平衡常数表达式K= 。能否由题给条件判断K值随温度变化是增大还是减小 (选填“能”或“不能”)。
(2)表中,a=
mol·L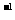 。50℃时,K=
。50℃时,K= ,在20min时,反应是否达到平衡 (选填“是”或“否”)。
,在20min时,反应是否达到平衡 (选填“是”或“否”)。
(3)在10-20min时,用乙醇表示的平均反应速率为
mol·L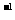 ·min
·min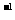 。该反应速率比0-10min的平均反应速率小,其原因是
。该反应速率比0-10min的平均反应速率小,其原因是
。
(4)在起始浓度相同的情况下,要提高甲酸乙酯的产率,可采取的措施是
。


 ,它的分子式为
,它
芳香族化合物(填“属于”或“不属于”)
,它的分子式为
,它
芳香族化合物(填“属于”或“不属于”) (填“增大”、“减小”或“不变”);
(填“增大”、“减小”或“不变”); ) ;
) ; 2NH3(g)。已知,在常温下,1g H2完全转化为NH3,放出的热量为15.4 kJ。①请写出该反应的热化学方程式 。常温下,将10mol N2和30mol H2放入合成塔中,充分反应,则放出的热量 (填“等于”、“大于”或“小于”)924 kJ。
2NH3(g)。已知,在常温下,1g H2完全转化为NH3,放出的热量为15.4 kJ。①请写出该反应的热化学方程式 。常温下,将10mol N2和30mol H2放入合成塔中,充分反应,则放出的热量 (填“等于”、“大于”或“小于”)924 kJ。 =2H+,则阴极的电极反应式为
=2H+,则阴极的电极反应式为

 qC(g)△H<0的可逆反应,在一定温度下的密闭容器中进行,平衡时B的体积分数V(B)%与压强(P)关系如下图所示,下列叙述正确的是
qC(g)△H<0的可逆反应,在一定温度下的密闭容器中进行,平衡时B的体积分数V(B)%与压强(P)关系如下图所示,下列叙述正确的是