网址:http://m.1010jiajiao.com/timu_id_1729733[举报]
氨的工业合成工艺的成熟推动了人类文明的进步,不少科技工作者为了寻找廉价的氨的制备方法,进行了前赴后继的探索性工作。请回答下列各题:
用氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2+3H2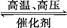 2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
(1)请写出该反应的热化学方程式 。
(2)如果一个反应的ΔH-TΔS<0,则该反应能够自发进行。已知该反应的ΔS="-198.2" J·K-1·mol-1。则上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。
氨的工业合成工艺的成熟推动了人类文明的进步,不少科技工作者为了寻找廉价的氨的制备方法,进行了前赴后继的探索性工作。请回答下列各题:
用氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2+3H2 2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
(1)请写出该反应的热化学方程式 。
(2)如果一个反应的ΔH-TΔS<0,则该反应能够自发进行。已知该反应的ΔS=-198.2 J·K-1·mol-1。则上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。
查看习题详情和答案>>
氨的工业合成工艺的成熟推动了人类文明的进步,不少科技工作者为了寻找廉价的氨的制备方法,进行了前赴后继的探索性工作。请回答下列各题:
(1)用氢气和氮气合成氨是一个可逆反应,化学方程式如下:N2(g)+3H2(g) ![]() 2NH3(g)。已知,在常温下,1g H2完全转化为NH3,放出的热量为15.4kJ。
2NH3(g)。已知,在常温下,1g H2完全转化为NH3,放出的热量为15.4kJ。
①请写出该反应的热化学方程式 。常温下,将10mol N2和30mol H2放入合成塔中,放出的热量 (填“大于”或“大于”或“小于”)924 kJ
②如果一个反应的△H-T△S<0,则该反应能够自发进行。已知该反应的△S=-198.2J?K-1?mol-1。请判断上述氨气的合成反应在常温下 (填“能”或“不能”)自发进行。(2)Marnellos和Stoukides发明了电化学制备氨气方法,该方法用SCY陶瓷将阳极和阴极隔开,SCY陶瓷具有高质子导电性,其作用是传递H这种方法实现了高温常压下高转化率的电化学合成氨。已知阳极发生的电极反应为:H2→2H++2e-。则阴极的电极反应为 。
查看习题详情和答案>> 2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。
2NH3。已知,在常温下,1 g H2完全转化为NH3,放出的热量为15.4 kJ。