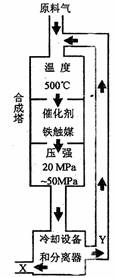
20.(8分)有一无色透明溶液,欲确定含有下列离子中的哪几种:
K+、Mg2+、Al3+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-。取该溶液实验如下:
|
实验步骤 |
实现现象 |
|
(1)取少量该溶液,加几滴甲基橙 |
溶液变红色 |
|
(2)取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热 |
有无色气体产生,气体遇空气变成红棕色 |
|
(3)取少量该溶液,加足量BaCl2溶液 |
有白色沉淀生成 |
|
(4)取(3)中上层清液,加AgNO3溶液 |
有稳定的白色沉淀生成,且不溶于HNO3 |
|
(5)取少量该溶液,加NaOH溶液 |
有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
由此判断:
(1)溶液中肯定存在的离子是 ,溶液中肯定不存在的离子是 。
(2)为进一步确定其他离子,应该补充的实验及对应欲检验离子的名称:
13.对下列各种溶液中所含离子的判断合理的是 ( )
A.向无色溶液中加氯水变橙色,溶液中可能含:Cl-、Br-、H+、Cu2+
B.在常温下加入铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,NO3-
C.常温,在c(H+)=10-14mol/L的溶液中可能含:Na+,AlO2-,CO32-,SO32-
D.使紫色石蕊试液变蓝色的溶液中可能含:K+,Na+,Ca2+,CO32-
|
|
C3N3(OH)3 3HNO3; 8HNCO+6NO2 7N2+8CO2+4H2O
下列说法正确的是 ( )
A.C3N3(OH)3与HNCO互为同分异构体
B.HNCO是一种很强的氧化剂
C.1mol NO2在反应中转移的电子为4mol
D.反应中NO2是还原剂
10.已知:CH3CH2CH3(g)+6.5O2(g)→4CO2(g)+5H2O(l);△H=-2878kJ/mol
(CH3)2CHCH3(g)+6.5O2(g)→4 CO2(g)+5H2O(l);△H=-2869kJ/mol
|
A.正丁烷的燃烧热为2878kJ
B.正丁烷分子储存的能量大于异丁烷分子
C.异丁烷转化为正丁烷的过程是一个放热过程
D.异丁烷分子中的碳氢键比正丁烷的多