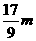17.(09广东化学 22)(12分)
22)(12分)
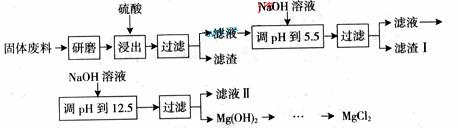
 某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、 CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:
某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、 CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:

|
沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
PH |
3.2 |
5.2 |
12.4 |
 部分阳离子以氢氧化物形式完全深沉时溶液的pH由见上表,请回答下列问题:
部分阳离子以氢氧化物形式完全深沉时溶液的pH由见上表,请回答下列问题:
 (1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有
(要求写出两条)。
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有
(要求写出两条)。
 (2)滤渣I的主要成分有 。
(2)滤渣I的主要成分有 。
 (3)从滤渣Ⅱ中可回收利用的主要物质有 。
(3)从滤渣Ⅱ中可回收利用的主要物质有 。
 (4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
(4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
 MgCl2+2NaClO3===Mg(ClO3)2+2NaCl
MgCl2+2NaClO3===Mg(ClO3)2+2NaCl
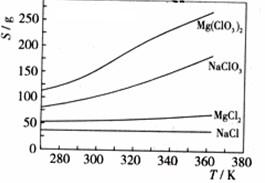
 已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:
已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:


 ①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2。简述可制备Mg(ClO3)2的原因:
。
①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2。简述可制备Mg(ClO3)2的原因:
。
 ②按①中条件进行制备实验。在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:
。除去产品中该杂质的方法是:
。
②按①中条件进行制备实验。在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是:
。除去产品中该杂质的方法是:
。
 答案:
答案:
(1)升高温度、搅拌、过滤后再向滤渣中加入硫酸(多次浸取)
 (2)Fe(OH)3 Al(OH)3
(2)Fe(OH)3 Al(OH)3
 (3)Na2SO4
(3)Na2SO4
 (4)①在某一时NaCl最先达到饱和析出;Mg(ClO3)2的溶解度随温度变化最大;NaCl 的溶解度与其他物质的溶解度有一定的差别。
(4)①在某一时NaCl最先达到饱和析出;Mg(ClO3)2的溶解度随温度变化最大;NaCl 的溶解度与其他物质的溶解度有一定的差别。
 ②降温前溶液中NaCl以达饱和;降低过程中NaCl溶解度会降低 ,会少量析出。重结晶。
②降温前溶液中NaCl以达饱和;降低过程中NaCl溶解度会降低 ,会少量析出。重结晶。
 解析:
解析:
浸出步骤硫酸同固体废料中主要成份反应,从化学反应速率和化学平衡的影响因素来看,可通过升高温度提高硫酸镁的溶解度,或通过搅拌使反应物充分接触反应,或通过过滤后滤渣多次浸取以提高转化率。硫酸浸出液经过滤,滤液中主要溶质是MgSO4、Al2(SO4)3和Fe2(SO4)3,根据阳离子以氢氧化物形式完全沉淀时溶液的pH,在调节pH至5.5时,Fe3+和Al3+已经完全沉淀,滤渣I的主要成分是Fe(OH)3 Al(OH)3,此时滤液中阴离子主要是SO42-,加入NaOH后Mg2+完全沉淀,溶质主要成分是Na2SO4;反应MgCl2+2NaClO3===Mg(ClO3)2+2NaCl类似于侯德榜制碱法生成NaHCO3的原理,因为NaCl溶解度小而从溶液中析出,使反应向生成Mg(ClO3)2的方向进行;同样是依据①的原理,在降温的过程中,Mg(ClO3)2的溶解度不断减小,从溶液中析出,在生成Mg(ClO3)2的过程中NaCl也不断生成,但因溶解度没有增加,所以也伴随Mg(ClO3)2析出;相同温度时氯化钠的溶解度最小,因此在冷却降温析出Mg(ClO3)2过程中一定会析出氯化钠。由于氯酸镁和氯化钠均溶于水,溶于水的可溶性物质一般用结晶和重结晶的方法分离。
16.(09广东化学21)(12分)
 三草酸合铁酸钾晶体K3 [Fe(C2O4 )3]·3H2O可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究。请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程。
三草酸合铁酸钾晶体K3 [Fe(C2O4 )3]·3H2O可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究。请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程。
 限选试剂:浓硫酸、1.0 mol·L-1HNO3、1.0 mol·L-1盐酸、1.0 mol·L-1 NaOH、3% H2O2 、0.1mol·L-1KI、0.1 mol·L-1CuSO4、20% KSCN、澄清石灰水、氧化铜、蒸馏水。
限选试剂:浓硫酸、1.0 mol·L-1HNO3、1.0 mol·L-1盐酸、1.0 mol·L-1 NaOH、3% H2O2 、0.1mol·L-1KI、0.1 mol·L-1CuSO4、20% KSCN、澄清石灰水、氧化铜、蒸馏水。
 (1)将气体产物依次通过澄清石灰水(A)、浓硫酸、灼热氧化铜(B)、澄清石灰水(C),观察到A、C中澄清石灰水都变浑浊,B中有红色固体生成,则气体产物是 。
(1)将气体产物依次通过澄清石灰水(A)、浓硫酸、灼热氧化铜(B)、澄清石灰水(C),观察到A、C中澄清石灰水都变浑浊,B中有红色固体生成,则气体产物是 。
 (2)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3。验证固体产物中钾元素存在的方法是
,现象是
。
(2)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3。验证固体产物中钾元素存在的方法是
,现象是
。
 (3)固体产物中铁元素存在形式的探究。
(3)固体产物中铁元素存在形式的探究。
 ①提出合理假设
①提出合理假设
 假设1:
;
假设2:
;假设3:
。
假设1:
;
假设2:
;假设3:
。
 ②设计实验方案证明你的假设(不要在答题卡上作答)
②设计实验方案证明你的假设(不要在答题卡上作答)
 ③实验过程
③实验过程
 根据②中方案进行实验。在答题卡上按下表的格式写出实验步骤、预期现象与结论。
根据②中方案进行实验。在答题卡上按下表的格式写出实验步骤、预期现象与结论。
 实验步骤 实验步骤 |
预期现象与结论 |
|
步骤1: |
|
|
步骤2: |
|
|
步骤3: |
|
|
…… |
|
 答案:
答案:
(1)CO2、CO
 (2)焰色反应 透过蓝色钴玻璃,观察到紫色的火焰
(2)焰色反应 透过蓝色钴玻璃,观察到紫色的火焰
 (3)①FeO FeO、Fe
Fe
(3)①FeO FeO、Fe
Fe
|
实验步骤 |
预期现象与结论 |
|
步骤1:取适量固体产物与试管中,加入足量蒸馏水,充分振荡使碳酸钾完全溶解。分离不容固体与溶液,用蒸馏水充分洗涤不溶固体 |
固体产物部分溶解 |
|
步骤2:向试管中加入适量硫酸铜溶液,再加入少量不溶固体,充分振荡 |
(1) 若蓝色溶液颜色及加入的不溶固体无明显变化,则假设2成立。 (2)  若蓝色溶液颜色明显改变,且有暗红色固体生成,则证明有铁单质存在 若蓝色溶液颜色明显改变,且有暗红色固体生成,则证明有铁单质存在 |
|
步骤3:继续步骤2中的(2),进行固液分离,用蒸馏水洗涤固体至洗涤液无色。取少量固体与试管中,滴加过量HCl,静置,取上层清液,滴加适量H2O2
,充分振荡后滴加KSCN |
结合步骤2中的(2): (1)  若溶液基本无色,则假设(1)成立 若溶液基本无色,则假设(1)成立(2)  若溶液呈血红色,则假设(3)成立 若溶液呈血红色,则假设(3)成立 |
 ③步骤1:将固体产物加入1.0 mol·L-1盐酸中 观察有无气体 若有气泡产生、说明固体产物中含有单质铁,反之,则不含单质铁
③步骤1:将固体产物加入1.0 mol·L-1盐酸中 观察有无气体 若有气泡产生、说明固体产物中含有单质铁,反之,则不含单质铁
 步骤2:将固体产物加入足量的0.1 mol·L-1CuSO4中充分反应后过滤、洗涤后,将沉淀物溶于1.0 mol·L-1盐酸,再加入20% KSCN,最后加入3% H2O2,若最终溶液显红色,说明固体产物中含有FeO,若不出现红色、说明不含有FeO
步骤2:将固体产物加入足量的0.1 mol·L-1CuSO4中充分反应后过滤、洗涤后,将沉淀物溶于1.0 mol·L-1盐酸,再加入20% KSCN,最后加入3% H2O2,若最终溶液显红色,说明固体产物中含有FeO,若不出现红色、说明不含有FeO
 解析:
解析:
 (1)将产生的气体产物依次通过澄清石灰水,石灰水变混浊,说明产生的气体中含有CO2,然后再通过灼热氧化铜、澄清石灰水,观察到有红色固体生成,澄清石灰水都变浑浊,气体中含有CO;
(1)将产生的气体产物依次通过澄清石灰水,石灰水变混浊,说明产生的气体中含有CO2,然后再通过灼热氧化铜、澄清石灰水,观察到有红色固体生成,澄清石灰水都变浑浊,气体中含有CO;
(2)碱金属元素的检验一般采用焰色反应;
(3)依据信息:固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3,可推测铁元素只能以亚铁及铁单质的形式存在;在设计实验时,应注意Fe与FeO的性质的不同点。
13. (09天津卷
(09天津卷 7)(14分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
7)(14分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
 (2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
 (3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
 (4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
 a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
 (5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

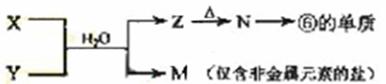
 X溶液与Y溶液反应的离子方程式为_____________________,
X溶液与Y溶液反应的离子方程式为_____________________,
 N→⑥的单质的化学方程式为________________。
N→⑥的单质的化学方程式为________________。
 常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
答案:


解析:
本题以周期表为题材,考查原子半径比较,酸性强弱,电子式,离子方程式以及盐类水解等知识。
(1)⑤⑥位于同一周期,且⑤排在⑥的前面,原子半径大,而④在上一周期,比⑤、⑥少一个电子层,故半径最小。
(2)②⑦位于同一主族,上面的非金属性强,最高价含氧酸酸性强,②③位于同一周期,且③在后,非金属性强,对应的酸性强。
(3)四种元素分别为氢、氧、钠和氯,离子键显然必须是钠盐,极性共价键则应有两种非金属组成。
(4)液态H2O2可以在MnO2、FeCl3等催化剂作用下发生分解反应。
(5)⑥为Al,可推断Z为Al(OH)3,受热分解可产物Al2O3,再电解即可得单质铝。M仅含非金属的盐,显然铵盐,所以X与Y应为AlCl3与NH3·H2O的反应,生成NH4Cl。由于NH4+ 水解,故要使其浓度与Cl-相等,则要补充NH3·H2O。由电荷守恒知:C(NH4+ )+ C(H+) C(Cl-)+C(OH-),若C(NH4+ )
C(Cl-)+C(OH-),若C(NH4+ )  C(Cl-),则C(H+)= C(OH-),即pH=7。
C(Cl-),则C(H+)= C(OH-),即pH=7。

 衡常数表达式为:K=
衡常数表达式为:K=

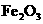 粉末的密闭容器中通入CO气体,10min后,生成了单
粉末的密闭容器中通入CO气体,10min后,生成了单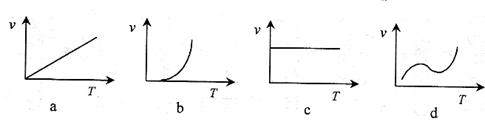
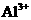 浓度增加,可加入的物质是
。
浓度增加,可加入的物质是
。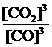
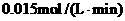
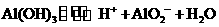 盐酸
(合理即给分)
盐酸
(合理即给分)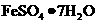 。
。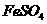 溶液与稍过量的
溶液与稍过量的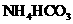 溶液混合,得到含
溶液混合,得到含 的浊液
的浊液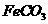 固体
固体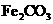 固体
固体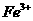 ,该反应的离子方程式是
,该反应的离子方程式是
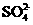 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 ,现煅烧464.0kg的
,现煅烧464.0kg的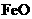 ,则该产品中
,则该产品中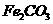 的质量是
kg(摩尔质量/g·
的质量是
kg(摩尔质量/g·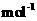 ;
;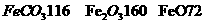 )
)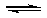 Fe(OH)2
+ 2H+的平衡向逆反应方向移动,从而抑制FeSO4的水解
Fe(OH)2
+ 2H+的平衡向逆反应方向移动,从而抑制FeSO4的水解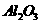 ,含
,含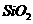 、
、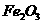 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下: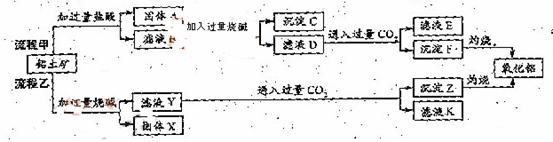
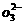 的离子方程式为________.
的离子方程式为________. 的容度积常数
的容度积常数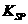 =5.6×
=5.6×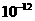 ,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的
,取适量的滤液B,加入一定量的烧碱达到沉淀溶液平衡,测得PH=13.00,则此温度下残留在溶液中的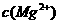 =_______.
=_______.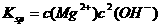 ,
,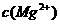 =5.6×10-12/(0.1)2=5.6×10-10。
=5.6×10-12/(0.1)2=5.6×10-10。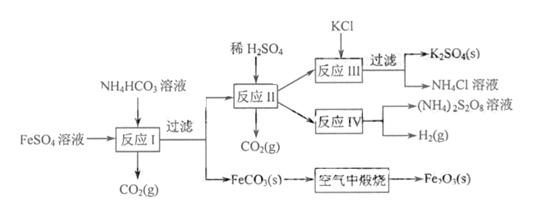
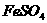 溶液中加入 ▲
(填字母),以除去溶液中的
溶液中加入 ▲
(填字母),以除去溶液中的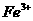 。
。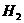
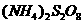 (过二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为
。
(过二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为
。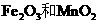 B.
B.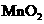 和
和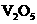 C.
C.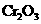 和
和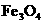 和FeO
和FeO (09上海卷
(09上海卷 B.
B.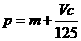 C.n=m+17Vc D.
C.n=m+17Vc D.
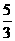 <
< 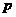 <
<