15.(10分)已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价Cr的强氧化性,其毒性是+3价Cr毒性的100倍。因此,必须对含铬的废水进行处理。目前研究和采用的处理方法主要有:
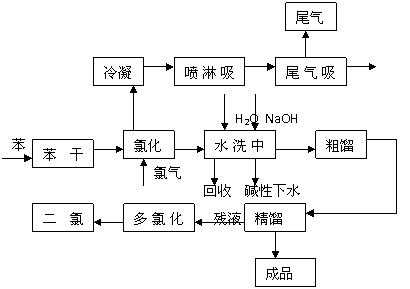
 方法一、还原法:在酸性介质中用FeSO4、NaHSO3等将+6价Cr还原成+3价Cr。具体流程如下:
方法一、还原法:在酸性介质中用FeSO4、NaHSO3等将+6价Cr还原成+3价Cr。具体流程如下:
有关离子完全沉淀的p H如下表。
|
|
Fe(OH)2 |
Fe(OH)3 |
Cr(OH)3 |
|
Ksp |
8.0×10-16 |
4.0×10-38 |
6.0×10-31 |
|
完全沉淀的pH |
9.0 |
3.2 |
5.6 |
请回答下列问题:
(1)在②中调节pH的范围至 为最好。(填序号)
A.3-4 B.6-8 C.10-11 D.12-14
(2)若在①使FeSO4适当过量、空气适量,使Fe2+与Fe3+的比例恰当时,可产生具有磁性、组成类似于Fe3O4•xH2O的铁氧体悬浮物,变废为宝。则控制空气适量的目的是 ,使铁氧体分离出来较简便的方法是 。
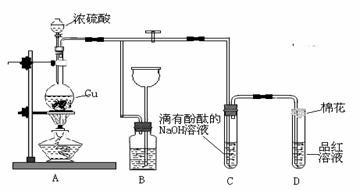
方法二、电解法:将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解:
阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3十在阴极区与OH一结合生成Fe(OH)3
和Cr(OH)3沉淀除去。
(3)写出此阴极反应的电极方程式 。现用上法处理1×104 L含铬(+6价)78 mg / L的废水,电解时阳极物质消耗的质量至少为________kg。


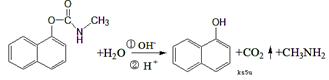 西维因是一种高效低毒杀虫剂,在一定条件下可水解:
西维因是一种高效低毒杀虫剂,在一定条件下可水解: 2HI(g),下列有关说法正确的是 ( )
2HI(g),下列有关说法正确的是 ( )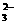
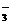 的溶液中:K+、OH-、NO
的溶液中:K+、OH-、NO