330. 市场销售的某种食用精制盐包装袋上有如下说明(部分):
|
产品标准 |
 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
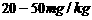 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处): 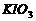 +
+
 +
+ 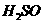 4
=
4
= 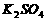 +
+
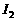 +
+ 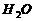
(2)上述反应生成的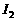 可用四氯化碳检验。向碘的四氯化碳溶液中加入
可用四氯化碳检验。向碘的四氯化碳溶液中加入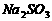 稀溶液,将
稀溶液,将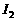 还原,以回收四氯化碳。
还原,以回收四氯化碳。
①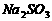 稀溶液与
稀溶液与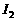 反应的离子方程式是
反应的离子方程式是

②某学生设计回收四氯化碳的操作步骤为:
a、将碘的四氯化碳溶液置于分液漏斗中; b、加入适量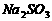 稀溶液;
稀溶液;
、分离出下层液体。
以上设计中遗漏的操作及在上述操作中的位置是
(3)已知: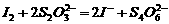
某学生测定食用精制盐的碘含量,其步骤为:
a、准确称取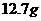 食盐,加适量蒸馏水使其完全溶解;
食盐,加适量蒸馏水使其完全溶解;
b、用稀硫酸酸化所得溶液,加入足量 溶液,使食用盐中
溶液,使食用盐中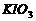 与
与 反应完全;
反应完全;
、以淀粉溶液为指示剂,逐滴加入物质的量浓度为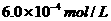 的
的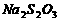 溶液
溶液 ,恰好反应完全。
,恰好反应完全。
①判断中反应恰好完全依据的现象是
②根据以上实验和包装说明,所测精盐的碘含量是 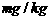
贵州省贵阳一中2011届高三化学一轮复习专题题库:
326. 已知下述三个实验均能发生化学反应
|
① |
② |
③ |
|
将铁钉放入硫酸铜溶液中 |
向硫酸亚铁溶液中滴入几滴浓硝酸 |
将铜丝放入氯化铁溶液中 |
下列判断正确的是( )
A.上述实验证明氧化性:Fe3+>Fe2+>2+
B.实验②中Fe2+既显氧化性又显还原性
.实验③中发生是置换反应
D.实验①中铁钉只做还原剂
 2↑+32↑被还原的元素是()
2↑+32↑被还原的元素是() 、的还原性由强到弱的顺序是()
、的还原性由强到弱的顺序是() n4溶液中滴加盐酸,Mn4溶液褪色
n4溶液中滴加盐酸,Mn4溶液褪色 3+>I2
3+>I2 (3)2Mn4+16Hl=2l+2Mnl2+l2+8H2
(3)2Mn4+16Hl=2l+2Mnl2+l2+8H2
 H-
H- 氯元素质量的倍
氯元素质量的倍 2Mn4+Mn2+2↑
2Mn4+Mn2+2↑ 。
。
 l3+ Hl(浓)= l+ l2↑+
l2↑+ H2
l3+ Hl(浓)= l+ l2↑+
l2↑+ H2 是___________(填编号)
是___________(填编号) .........m
.........m