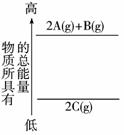
6.(2009年珠海模拟)在一定条件下发生化学反应:2SO2(g)+O2(g)=2SO23(g);ΔH=-197 kJ·mo-1L现有容积相同的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
|
容器 |
SO2(mol) |
O2(mol) |
N2(mol) |
Q(kJ) |
|
甲 |
2 |
1 |
0 |
Q1 |
|
乙 |
2 |
1 |
0 |
Q2 |
|
丙 |
1 |
0.5 |
1 |
Q3 |
根据以上数据,下列叙述不正确的是( )
A.在上述条件下反应生成1 mol SO23气体放热98.5 kJ
B.上述条件下每摩尔该反应进行到底时放出的热量为197 kJ
C.Q1=2Q2=2Q3=197 kJ
D.2Q2=2Q3<Q1<197 kJ
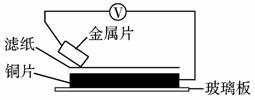
12.(2009年枣庄质检)将洁净的金属片A、B、C、D分别放置在浸有食盐溶液的滤纸上面并压紧(如下图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下:
|
金属 |
电流方向 |
电压(V) |
|
A |
Cu→A/ |
+0.78 |
|
B |
B→Cu |
-0.15 |
|
C |
Cu→C |
+1.35 |
|
D |
Cu→D |
+0.30 |
已知:构成两电极的金属活动性相差越大,电压表的读数越大。请依据表中数据判断:
(1)____________金属可能是最强的还原剂。
(2)____________金属一定不能从硫酸铜溶液中置换出铜。
(3)若滤纸不用盐溶液浸润而改用NaOH溶液浸润,则在滤纸上能看到有蓝色沉淀析出的是____________(填字母)。金属对应的原电池的电极反应为:
负极:______________,