12.下表是铬酸(H2CrO4)溶液中离子的组成与pH的关系,请回答下列问题:
|
pH |
[CrO42-] |
[HCrO4-] |
[Cr2O72-] |
[H2CrO4] |
|
4 |
0.0003 |
0.104 |
0.448 |
0 |
|
5 |
0.0033 |
0.103 |
0.447 |
0 |
|
6 |
0.0319 |
0.0999 |
0.437 |
0 |
|
7 |
0.2745 |
0.086 |
0.3195 |
0 |
|
8 |
0.902 |
0.0282 |
0.0347 |
0 |
|
9 |
0.996 |
0.0031 |
0.0004 |
0 |
(1)写出铬酸电离反应方程式:____________ ____________ 。
(2)若要得到CrO42-应控制的条件是____________ 。
(3)铬酸(H2CrO4)溶液中,电离出CrO42-的电离平衡常数为K2,电离出Cr2O72-的电离平衡常数为K3,则K2__________K3(填“>”、“=”或“<”)。
(4)铬酸的物质的量浓度为____________(精确到小数点后两位)。
9.对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。若25 ℃时有HA=H++A-,则K=c(H+)·c(A-)/c(HA)式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25 ℃):
|
酸 |
电离方程式 |
电离平衡常数K |
|
CH3COOH |
CH3COOH=CH3COO-+H+ |
1.76×10-5 |
|
H2CO3 |
H2CO3=H++HCO3-
HCO3-=H++CO32- |
K1=4.31×10-7 K2=5.61×10-10 |
|
H2S |
H2S=H++HS HS-=H++S2- |
K1=9.1×10-8 K2=1.1×10-12 |
|
H3PO4 |
H3PO4=H++H2PO4-
H2PO4-=H++HPO42- HPO2-4=H++PO43- |
K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 |
回答下列各题:
(1)K只与温度有关,当温度升高时,K值____________(填“增大”“减小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?____________ 。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是____________,最弱的是____________。
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是______________,产生此规律的原因是____________ ____________ 。
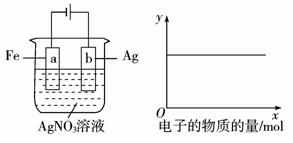 ①c(Ag+) ②c(NO3-)
①c(Ag+) ②c(NO3-)