19.现有四种短周期元素的有关信息如下表所示:
|
元素 |
结构特点及在周期表中的位置 |
单质及化合物的部分性质与用途 |
|
甲 |
在元素周期表中,主族序数等于周期数 |
工业上用电解法冶炼该金属 |
|
乙 |
单质的晶体类型为原子晶体 |
氧化物是工业制普通玻璃的主要原料 |
|
丙 |
原子最外层电子数是最内层电子数的2倍 |
单质存在多种同素异形体 |
|
丁 |
元素能形成两种不同的阴离子 |
丁的一种单质与KI溶液反应生成另一种丁的单质 |
则甲、乙、丙、丁四种元素的原子序数从大到小排列的是 ( )
A.甲、乙、丙、丁 B.丁、甲、乙、丙
C.丙、丁、甲、乙 D.乙、甲、丁、丙
[答案]B
[解析]根据表中信息,甲是Al,乙是Si,丙是C,丁是O,丁的一种单质与KI溶液反应生成另一种丁的单质的化学方程式可表示为O3+2KI+H2O =2KOH+O2+I2。由此可知选项D正确。
[考点]物质结构、元素周期律
14.下列关于四个图像的说法正确的是 ( )
|
|



① ②


③ ④
A.图①表示化学反应中能量的变化,反应CO(g)+H2O(g)= CO2(g)+H2(g)的△H>0
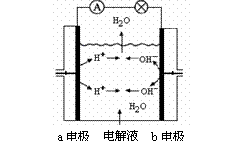
B.图②为氢氧燃料电池示意图,正、负极通入的气体体积之比为2︰1
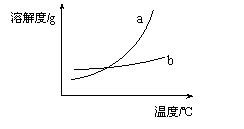
C.图③表示物质a、b的溶解度曲线,可以用结晶方法从a、b 混合物中提纯a
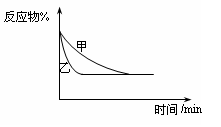
D.图④可以表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,且乙的压强大
3C(g)+D(s)的影响,且乙的压强大
[答案]C
[解析]图①表示反应物的总能量高于生成物的总能量,因此该反应为放热反应△H<0,A错。图② 氢氧燃料电池的总反应式为2H2+O2=2H2O,正极发生还原反应,通入O2,负极发生氧化反应,通入H2,故正负极通入的气体体积之比为1:2,B错,选项D注意到生成物D是固体,该反应是气体体积不等的反应,因此不合要求。应选C。
[考点]化学反应速率与化学平衡、电化学
 ( )
( )
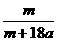 ×100%
B.
×100%
B.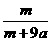 ×100%
×100%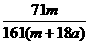 ×100%
D.
×100%
D.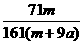 ×100%
×100% 2H2↑+O2↑,该反应中共转移4mol电子,因此当有amol电子转移时,电解过程中共消耗0.5amol的水,由于原溶液是饱和溶液,电解后的溶液也是饱和溶液,故饱和溶液质量分数的计算可作如下转化:mg晶体中Na2SO4的质量溶解在mg晶体中的水和0.5amol水中恰好饱和,由此可计算得选项D正确。
2H2↑+O2↑,该反应中共转移4mol电子,因此当有amol电子转移时,电解过程中共消耗0.5amol的水,由于原溶液是饱和溶液,电解后的溶液也是饱和溶液,故饱和溶液质量分数的计算可作如下转化:mg晶体中Na2SO4的质量溶解在mg晶体中的水和0.5amol水中恰好饱和,由此可计算得选项D正确。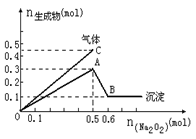
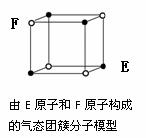 B.1mol金刚石晶体中,平均含有2mol C-C键
B.1mol金刚石晶体中,平均含有2mol C-C键