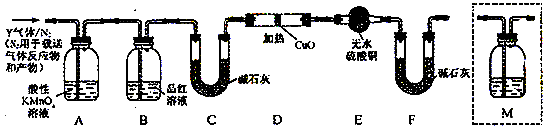
31.现有等物质的量的KHCO3和NaHCO3的混合物a g与2 mol/L盐酸反应。题中涉及到的气体均以标准状况计。填空时,可用带字母的分式表示。
(1)该混合物中KHCO3和NaHCO3的质量比为______________。
(2)如果该混合物与盐酸恰好完全反应,则所用盐酸的物质的量是____________。
(3)如果盐酸过量,则生成CO2的体积是为______________L。
(4)如果反应后,混合物有剩余,盐酸量不足,除上述已知条件外,还应知道下列条件中的______________,才能计算生成CO2的体积。
A.盐酸的体积 B.盐酸的密度和质量分数 C.盐酸的质量
(5)如果KHCO3和NaHCO3不是以等物质的量混合,a g固体混合物与足量盐酸完全反应生成CO2,求CO2的体积(V)的取值范围,写出简明的计算过程。
|

|
版权所有:()
版权所有:()
 上海交通大学附属中学2010-2011学年度第一学期
上海交通大学附属中学2010-2011学年度第一学期
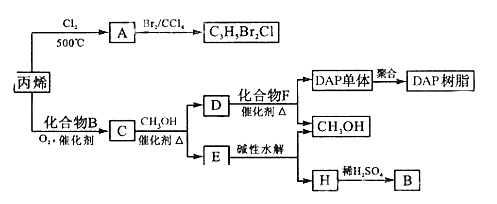
 RCOOR”+R’OH(R、R’、R”代表烃基)
RCOOR”+R’OH(R、R’、R”代表烃基)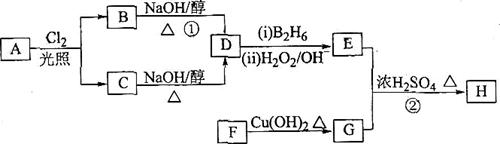
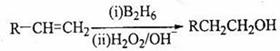 (B2H6为乙硼烷)。
(B2H6为乙硼烷)。