8.主族元素W、X、Y、Z位于同一周期,原子序数依次增大,W、X是金属元素,Y、Z是非金属元素。W、X的最高价氧化物对应的水化物可以相互反应, W与Y 可形成化合物W2Y,Y的最外层电子数是核外电子层数的2倍。下列说法正确的是
A.Y的气态氢化物比Z的气态氢化物稳定
B.W的最高价氧化物对应的水化物是最强的碱
C.Y单质和氧气、氢气都能发生化合反应,且产物都具有还原性
D.W、X、Y、Z四种元素的原子半径由小到大的顺序是:W<X<Y<Z
|
|




|
|
|
|
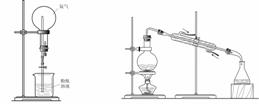

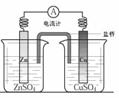
28. (16分)纯碱、烧碱等是重要的化工原料。
⑴利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 ;
若其它操作不变,将A与C连接,可观察到的现象是 。
⑵向100mL 2mol/L的NaOH溶液中通入一定量CO2,低温结晶,得到9.3g白色固体,该白色因体的组成是 (写化学式)。请你设计实验确定该白色固体存在的阴离子,试完成下列方案:
|
实验操作 |
实验现象 |
结论 |
|
①取少量白色固体于试管中,加适量水溶解,再加足量BaC12溶液 |
|
|
|
②过滤,取2mL滤液于试管中 |
 |
 |
|
③ |
|
|
27.(16分) X、Y、Z、Q、R五种元素原子序数依次增大,且X和Y,Z和Q分别同周期,Q、R同主族且相邻,X的低价氧化物与Y单质分子的电子总数相等,Z和Q的核电荷数相差4,Q的2价简单离子与Ar原子的电子层结构相同。根据以上信息填空:
(1)Q离子的结构示意图______________;R的元素符号为___________;
(2)Y的气态氢化物空间构型是_______________;X和Q形成的共价化合物的电子式是_________________,属于__________分子(填“极性”或“非极性”);
(3)Y的最高价氧化物对应的水化物的稀溶液与Z的单质反应时,Y被还原到最低价,该反应的化学方程式是 ;
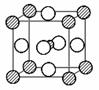
(4)据报道,只含Z、镍(Ni)和X三种元素的晶体竟然具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该晶体的晶胞结构如图,试写出该晶体的化学式 ;
|
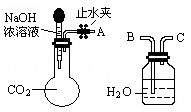 (5)核电荷数比Q多1的元素T,在298K时,T的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到T的最高价氧化物的水化物的稀溶液,并放出a kJ的热量。该反应的热化学方程式为 。
(5)核电荷数比Q多1的元素T,在298K时,T的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到T的最高价氧化物的水化物的稀溶液,并放出a kJ的热量。该反应的热化学方程式为 。
 A.石墨烯是一种有机物
A.石墨烯是一种有机物
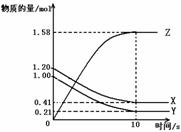 (12分)I.在温度为500K,2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:
(12分)I.在温度为500K,2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示: 球,镍原子用大
球,镍原子用大 球,Z原子用大
球,Z原子用大 球
球