21.(12分)
二氯化二硫(S2C12)在工业上用于橡胶的硫化。为在实验室合成S2C12,某化学研究性学习小组查阅了有关资料,得到如下信息:
① 将干燥的氯气在110℃ - 140℃与硫反应,即可得S2C12粗品。
② 有关物质的部分性质如下表:
|
物质 |
熔点/℃ |
沸点/℃ |
化学性质 |
|
S |
112.8 |
444.6 |
略 |
|
S2C12 |
-77 |
137 |
遇H2O生成HCl、SO2、S; 300℃以上完全分解; S2C12 + C12  2SCl2 2SCl2 |
设计实验装置图如下:
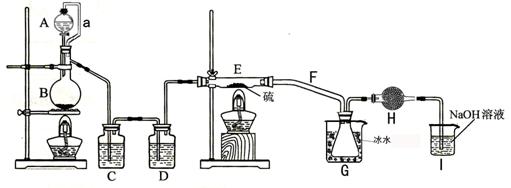
请回答下列问题:
①如何检查装置的气密性_________________________________________;
②装置中导管a的作用是_____ ____________;
③C、D中的试剂分别是_______________________、____________________;
④F导气管管径要大一些是为了防止____________________;
⑤S2C12粗品中可能混有的杂质是(填写两种化学式)______________、________________;
⑥如果没有H装置产率会大大降低,原因是___________ ;(用化学方程式表示)
⑦I中NaOH的作用是________________________。
19.(12分) 有A、B、C、D、E、F、G六种短周期元素,原子序数依次增大。
|
B |
C |
D |
|
|
G |
A元素的单质在自然界中最轻,B、C、D、G在周期表的位置如图,
它们的原子序数之和为37。E元素的电负性在同周期中最小,F
是同周期中原子半径最小的金属元素。试回答:
(1)A2D、A2G沸点较高的是__ (填化学式),原因是 ;
(2)E位于元素周期表第_____周期第________族,F原子结构示意简图为: ,G的基态原子核外电子排布式是 ;
(3)将0.1mol·L-1 G的最高价氧化物的水化物溶液逐滴滴入由B、D、E三种元素组成的无机盐溶液中,则刚开始时发生反应的离子方程式为 ;
(4)C与A形成10电子化合物的电子式是 ,该化合物与D2在一定条件发生置换反应,在该反应中氧化剂与还原剂的物质的量之比为 ;
(5)已知16g单质G完全燃烧放出148kJ热量。写出单质燃烧的热化学方程式
18.(6分)有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3- ,取该溶液进行实验:
|
实验步骤 |
实验现象 |
|
(1)取少量该溶液,加几滴紫色石蕊试液 |
溶液先变红 |
|
(2)取少量该溶液加热浓缩,加Cu片和浓 H2SO4 ,加热 |
有无色气体产生,气体遇空气变成红棕色 |
|
(3)取少量该溶液,加BaCl2溶液 |
有白色沉淀 |
|
(4)取(3)中上层清液,加AgNO3溶液 |
有白色沉淀,且不溶于稀HNO3 |
|
(5)取少量该溶液,加NaOH溶液 |
有白色沉淀,NaOH过量时沉淀部分溶解 |
由此判断:
(1)溶液中肯定不存在的离子有 ,溶液中肯定存在的离子是 。
(2)请设计实验验证其中可能存在的阴离子的方法(写明操作、现象、结论)
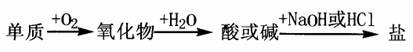 能实现下列物质间直接转化的元素是 ( )
能实现下列物质间直接转化的元素是 ( )
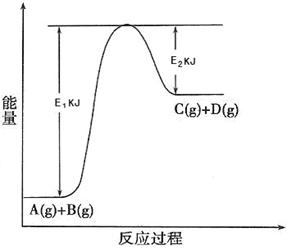
 C(g) +D(g) 过程中的能量变化如图所示,回答下列问题。
C(g) +D(g) 过程中的能量变化如图所示,回答下列问题。