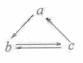
2.(姜堰市罗塘中学2009-2010学年第一学期期中考试高三化学试题)下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
|
a |
b |
c |
|
A |
Al |
AlCl3 |
 Al(OH)3 Al(OH)3 |
|
B |
NO |
NO2 |
HNO3 |
|
C |
Si |
SiO2 |
H2SiO3 |
|
D |
H2SO4 |
SO2 |
SO3 |
9.(江苏省黄桥中学2010届高三期中考试(化学))根据下列短周期元素性质的数据判断,下列说法正确的是
 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
原子半径/10-10 m |
0.66 |
1.36 |
1.23 |
1.10 |
0.99 |
1.54 |
0.70 |
1.18 |
|
最高或最低化合价 |
|
+2 |
+1 |
+5 |
+7 |
+1 |
+5 |
+3 |
|
-2 |
|
|
-3 |
-1 |
|
-3 |
|
A.元素①⑧形成的化合物具有两性 B.元素⑦位于第二周期Ⅴ族
C.元素④⑤形成的化合物是离子化合物 D.元素③的最高价氧化物对应水化物碱性最强
7.(江苏省高淳中学2010届高三上学期调研(化学))放射性的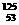 I对治疗肿瘤有一定疗效。该原子的原子核内的中子数是
I对治疗肿瘤有一定疗效。该原子的原子核内的中子数是
|
A.19 |
B.53 |
C. 72 |
D.125 |

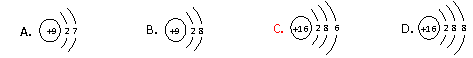
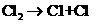 ②
②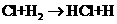 ③
③ ……
……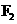 、
、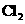 、
、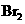 、
、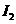 的顺序由难变易
的顺序由难变易 ……………………………………………………………1分
……………………………………………………………1分