0 33412 33420 33426 33430 33436 33438 33442 33448 33450 33456 33462 33466 33468 33472 33478 33480 33486 33490 33492 33496 33498 33502 33504 33506 33507 33508 33510 33511 33512 33514 33516 33520 33522 33526 33528 33532 33538 33540 33546 33550 33552 33556 33562 33568 33570 33576 33580 33582 33588 33592 33598 33606 447348
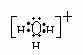 (12分)(1)[Ag(NH3)2]+, Fe(SCN)3
(12分)(1)[Ag(NH3)2]+, Fe(SCN)3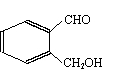 某有化合物的结构简式如图所示,回答下列各题:
某有化合物的结构简式如图所示,回答下列各题: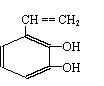
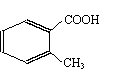
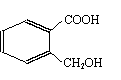 (2) )该有机物有多种同分异构体,下列结构的有机物不是它的同分异构体的是:___________
(2) )该有机物有多种同分异构体,下列结构的有机物不是它的同分异构体的是:___________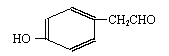
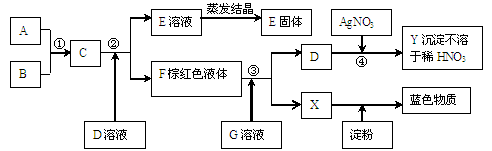
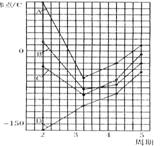 Ⅰ右图中A、B、C、D四条曲线是表示
Ⅰ右图中A、B、C、D四条曲线是表示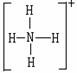
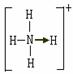 Ⅱ.已知氨分子内键与键的夹角约为107º18’。从反应NH3 +H+→NH4+可知:NH4+中有一根键比较特殊,其结构可表示为A式。但是,虽然有一根键形成过程与众不同,而其结果是完全相同的,都是N、H原子间共用一对电子,键与键的夹角均为109º28’。故NH4+的结构也可表示为B式。
Ⅱ.已知氨分子内键与键的夹角约为107º18’。从反应NH3 +H+→NH4+可知:NH4+中有一根键比较特殊,其结构可表示为A式。但是,虽然有一根键形成过程与众不同,而其结果是完全相同的,都是N、H原子间共用一对电子,键与键的夹角均为109º28’。故NH4+的结构也可表示为B式。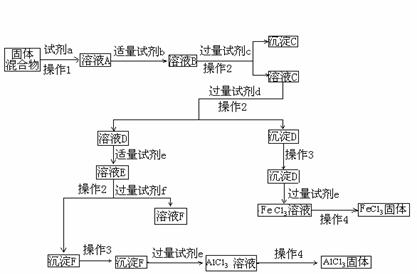 固体AlCl3和FeCl3混合物中含有少量FeCl2和Al2(SO4)3。某同学设计如下实验进行分离,以分别得到纯净的AlCl3和FeCl3固体。
固体AlCl3和FeCl3混合物中含有少量FeCl2和Al2(SO4)3。某同学设计如下实验进行分离,以分别得到纯净的AlCl3和FeCl3固体。 2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A 2 mol
B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3
mol/(L·min)。N:2 mol C y mol D;达平衡时c(A)=0.6 mol/L。下列推断的结论中不正确的是
2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A 2 mol
B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3
mol/(L·min)。N:2 mol C y mol D;达平衡时c(A)=0.6 mol/L。下列推断的结论中不正确的是