(二)某农资商店出售一种化肥,其有效成分为氯化铵,现欲测定该种化肥中氮元素的质量分数,设计实验步骤如下(杂质中不含氮元素,且杂质均不与盐酸或氢氧化钠溶液反应):
①配制1.00mol/L的HCl溶液和1.00mol/L的NaOH溶液;
②每次取1.00g此化肥样品,溶于20mL蒸馏水中;
③加入30.00mL1.00mol/L的NaOH溶液,将反应后的溶液加热煮沸约1分钟,冷却至常温;
④……………………;
⑤重复②③④步操作1-2次;
⑥记录整理实验所得数据,计算该化肥中氮元素的质量分数。
请回答下列问题:
(1)写出步骤④中的实验内容 ,写出实验步骤④中的离子方程式: 。
(2)步骤⑤的实验目的是 。
(3)若以Vx(mL)表示实验所测定消耗盐酸数据的平均值,该化肥样品中氮元素的质量分数计算表达式为 。(不需要化简)
17.(14分)在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液变为黄色。
(1)甲同学认为这不是发生化学反应所致,使溶液变黄色的物质是: (填粒子的化学式,下同);
乙同学认为这是发生化学反应所致,使溶液变黄色的物是
(2)现提供以下试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液
请判断哪位同学的推断是正确的,并用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
|
同学正确 |
选用试剂 |
实验现象 |
|
第一种方法 |
|
|
|
第二种方法 |
|
|
(3)若选用淀粉碘化钾溶液来判断哪位同学的推断是正确的,你认为是否可行? 理由是:
根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,首先被氧化的离子是 写出在稀溴化亚铁溶液中通入足量氯气时的离子方程式:
14.有甲、乙两位同学,他们一起做了水果电池的实验,测得数据如下:
|
实验次数 |
电极材料 |
水果品种 |
电极间 距/cm |
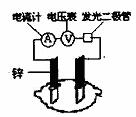 电压 电压/mV |
|
|
1 |
锌 |
铜 |
菠萝 |
3 |
900 |
|
2 |
锌 |
铜 |
苹果 |
3 |
650 |
|
3 |
锌 |
铜 |
柑 |
3 |
850 |
|
4 |
锌 |
铜 |
西红柿 |
3 |
750 |
|
5 |
锌 |
铝 |
菠萝 |
3 |
650 |
|
6 |
锌 |
铝 |
苹果 |
3 |
450 |
甲同学提出的问题,乙同学解释不正确的是
|
|
甲同学 |
乙同学 |
|
A |
实验6中的负极电极反应如何写? |
铝为负极:Al-3e-=Al3+ |
|
B |
实验1,5电流方向为什么相反? |
1中锌为负极,电流由铜经导线到锌,5中铝为负极,铝失去电子,电流由锌经导线流向铝 |
|
C |
水果电池的电压与哪些因素有关? |
只跟水果的类型有关 |
|
D |
实验中发光二极管不太亮,如何使它更明亮起来? |
可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来 |
12. 一些烷烃的燃烧热(KJ/mol)如下表:
|
化合物 |
燃烧热 |
化合物 |
燃烧热 |
|
甲烷 |
891.0 |
正丁烷 |
2878.0 |
|
乙烷 |
1560.8 |
异丁烷 |
2869.6 |
|
丙烷 |
2221.5 |
2-甲基丁烷 |
3531.3 |
下列表达正确的是
A.热稳定性:正丁烷<异丁烷
B.乙烷燃烧的热化学方程式为:
2C2H6(g)+7O2(g)=4CO2(g)+6H2O(g) ΔH=-1560.8KJ/mol
C.正戊烷的燃烧热大约在3540 KJ/mol左右
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
 [Cu(NH3)3]Ac·CO+Q
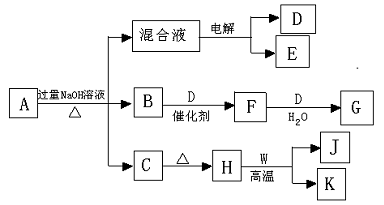
[Cu(NH3)3]Ac·CO+Q (12分)有一化合物A ,其水溶液为浅绿色,可发生如下的转化关系。其中B、D、E为无色气体,W、K为常见的金属单质, C为难溶于水的红褐色固体。在混合液中加入BaCl2可生成不溶于稀HNO3的白色沉淀,H和W反应可放出大量的热。
(12分)有一化合物A ,其水溶液为浅绿色,可发生如下的转化关系。其中B、D、E为无色气体,W、K为常见的金属单质, C为难溶于水的红褐色固体。在混合液中加入BaCl2可生成不溶于稀HNO3的白色沉淀,H和W反应可放出大量的热。