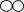3.CaCl2溶液呈中性。
(1)滤渣B中一定含有_____,产生该物质的化学方程式可能是_____(写出一个即可)。
(2)滤液C成分的探究。
[猜想]滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Ca(OH)2;④____。
[设计方案并进行实验]甲、乙、丙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3。
乙同学:取滤液C少许放入试管中,滴加足量的无色酚 酞,液体变成红色,则滤液C中的溶质一定含有NaOH。
酞,液体变成红色,则滤液C中的溶质一定含有NaOH。
丙同学:取滤液C少许放入试管中,滴加Ca(OH)2溶液,有白色沉淀产生。向上层清液中滴加无色酚酞,无色酚酞变成红色,则滤液C中的溶质是NaOH和Na2CO3。
[反思与评价]
丁同学认真分析上述三位同学的实验,认为他们的结论均有不足之处,并且做出了正确的判断。他认为滤液C中的溶质一定含有________,可能含有NaOH。为进一步确认滤液C中是否含NaOH,请你帮助他设计实验进行验证。
|
实验操作 |
实验现象 |
实验结论 |
|
|
|
猜想④正确 |
(3)实验过程中,同学们还发现向样品中加入足量水溶解时放出大量的热。综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是__________(填序号)。
① 样品中一定含NaOH ② 样品中一定含Na2CO3
③ 样品中含NaOH、CaO中的一种或两种
33.(7分)实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物。同学们为
 确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究。
确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究。
|
|||
|
查阅资料:1.Ca(OH)2、Na2CO3溶于水无明显的温度变化。
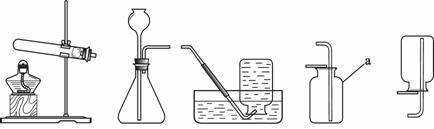
31.(6分)实验室制取气体所需装置如下图所示。
A B C D E
请回答以下问题:
(1)装置中标“a”的仪器名称是__________。
(2)用高锰酸钾制取氧气时,所选用的发生装置是_____(填字母序号,下同),收集装置是C或_______。
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是_____,其反应的化学方程式为_______。该装置还可用于制氧气,其反应的化学方程式为_______。
32.(6分)学了炼铁原理后,小明想用此原理测定某一生锈铁粉中氧化铁的
质量分数。于是他取m1 g生锈的铁粉样品,按下图所示装置进行实验,测定该样品中氧化铁的质量分数(铁锈按氧化铁处理)。
|
(1)装置A中反应的化学方程式是___________________。
(2)某同学欲通过B装置反应前后的质量变化,测定该样品中氧化铁的质量分数。
B中的最佳试剂是_____(填序号),实验时B中反应的化学方程式是_____。
① 澄清石灰水 ② 氢氧化钠浓溶液 ③ 稀盐酸 ④ 水
(3)上述实验过程中,CO气体除作为反应物外,还能起到的作用是:① 实验开始时,排尽装置中的空气,防止加热时发生爆炸;② 停止加热后,防止A中生成物被氧化,B中的溶液倒吸入A中;③______________________。
(4)完全反应后,甲同学称得铁粉的质量为m2 g,同时测得装置B增重m3 g,则铁粉样品中氧化铁的质量分数为_____________________。
28.(6分)下列数据是硝酸钾固体在不同温度时的溶解度。
|
温度/℃ |
0 |
20 |
40 |
60 |
80 |
|
溶解度/g |
13.3 |
31.6 |
63.9 |
110 |
169 |
(1)硝酸钾的化学式为__________,期中氮元素的化合价为________,硝酸钾溶液中的溶剂是 。
(2)20℃时,向100 g水中加入31.6 g硝酸钾,充分溶解后得到 (填“饱和”或“不饱和”)溶液。
(3)20℃时,向100 g水中加入40 g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是 。
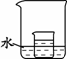 (4)右图所示,小烧杯中盛放的是(2)中所得的硝酸钾溶液。若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是 (填字母)。
(4)右图所示,小烧杯中盛放的是(2)中所得的硝酸钾溶液。若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是 (填字母)。
A.冰 B.干冰 C.硝酸铵
D.浓硫酸 E.氢氧化钠 F.氧化钙
26.(5分)化学与生活息息相关。
(1)某品牌“蛋黄派”主要营养信息如下图1所示。
①下图1中所含营养素主要有 种;
② 是人体所需能量的主要来源。

|
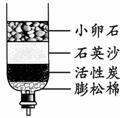
(2)将浑浊的河水用上图2所示的简易净水器进行净化,其中活性炭的作用是_____,用此装置净化后得到的水属于________(填“纯净物”或“混合物”)。
(3)下列生活用品,主要用有机合成材料制成的是_________(填字母序号)。




A.羊毛衫 B.涤纶连衣裙 C.腈纶运动衣 D.纯棉T恤