|
MgCl2 === Mg + Cl2↑。
某工厂要生产出120 t金属镁,至少需要电解氯化镁多少吨?
35.(3分)久置的氢氧化钠中常含有少量的碳酸钠。某实验小组取久置的氢氧化钠12 g,加65 g水完全溶解后,再缓慢加入25 g石灰乳(氢氧化钙和水的混合物),恰好完全反应。过滤得到沉淀质量为2 g。反应后所得溶液的溶质质量分数为多少?
海淀区九年级第二学期期中练习
33. (8分)小军家的下水管道堵了。爸爸买回一种“管道通”,使用后堵塞的管道畅通无阻了。小军对此很好奇,于是想探究“管道通”中的物质成分。
(8分)小军家的下水管道堵了。爸爸买回一种“管道通”,使用后堵塞的管道畅通无阻了。小军对此很好奇,于是想探究“管道通”中的物质成分。
[提出问题]“管道通”中的物质是什么?
[查阅资料]主要内容如下。
(1)下水管里的淤积物主要为油污、食物残渣、毛发等。
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西。常用于疏通管道。
(3)铝粉为银灰色固体。铝与酸、碱溶液都能反应放出氢气,反应时放出大量热。
①铝与盐酸反应的化学方程式是 。
②铝与氢氧化钠溶液反应的化学方程式是
2Al+2NaOH + ==2NaAlO2 +3H2↑
[猜想与验证]小军打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末。
(1)猜想:白色固体颗粒为氢氧化钠。
|
实验操作 |
实验现象 |
|
①将几粒白色固体颗粒放在表面皿上,放置一会儿。 |
。 |
|
②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁。 |
。 |
|
③向步骤②得到的溶液中放入一段羊毛线,加热一段时间。 |
羊毛线逐渐消失。 |
结论:白色固体颗粒为氢氧化钠。
(2)猜想:银灰色粉末为铝粉。
|
实验操作 |
实验现象 |
①按照下图安装两套仪器。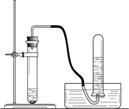 |
|
|
②两套仪器中分别依次加入银灰色粉末和稀盐酸;银灰色粉末和
。 |
都产生大量无色气体,试管外壁温度明显升高。 |
③待导管口有气泡均匀持续冒出时, 收集1试管气体,验纯。(两套仪器操作相同) 收集1试管气体,验纯。(两套仪器操作相同) |
验纯时的操作和现象:(两套仪器相同) 。 |
|
④在导管口点燃气体。(两套仪器操作相同) |
都产生淡蓝色火焰。 |
结论:银灰色粉末为铝粉。
[应用]使用管道通时,先将其中银灰色粉状固体添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水,堵上管道口。一会儿,管道内发生化学反应。根据题目信息,推测管道内的反应现象是 。
[反思]①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似。要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在。
②根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可) 。
30.(6分)现有生活中常见的四种未知白色粉末,它们分别是食盐、纯碱、去污粉(主要成分为碳酸钠和碳酸钙)和使用过的生石灰干燥剂。化学小组为了确定每种未知固体的成分,将它们分别标记为①、②、③、④后进行实验,实验现象记录如下:
|
实验过程 |
实验现象 |
|
实验1: 分别取样于四支试管中,加入足量的水充分溶解 |
②、③ 完全溶解,①、④ 均在试管底部有白色固体,且①中有明显放热 |
|
实验2:静置一段时间后,分别取上层清液,加入试剂A |
③、④均有气泡产生 |
|
实验3:分别取样于四支试管中,加入足量试剂A |
白色固体均消失;①③④均有气泡产生 |
根据以上实验现象,回答下列问题:
(1)实验1中,物质①发生反应的化学方程式是 。
(2)物质②为 ,试剂A为 。
(3)实验3中,试剂A与物质④发生反应的化学方程式是 。
(4)通过实验判断,物质①中一定含有的成分是 。
 氧气
C. 稀有气体 D. 二氧化碳
氧气
C. 稀有气体 D. 二氧化碳 (6分)为了验证二氧化碳与氢氧化钠可以发生化学反应,某小组用下图
(6分)为了验证二氧化碳与氢氧化钠可以发生化学反应,某小组用下图 所示装置进行实验。请回答下列问题:
所示装置进行实验。请回答下列问题: