摘要:28.下列数据是硝酸钾固体在不同温度时的溶解度. 温度/℃ 0 20 40 60 80 溶解度/g 13.3 31.6 63.9 110 169 (1)硝酸钾的化学式为 .期中氮元素的化合价为 .硝酸钾溶液中的溶剂是 . (2)20℃时.向100 g水中加入31.6 g硝酸钾.充分溶解后得到 溶液. (3)20℃时.向100 g水中加入40 g硝酸钾.若使硝酸钾完全溶解.可以采用的方法是 . (4)右图所示.小烧杯中盛放的是(2)中所得的硝酸钾溶液.若将少量的下列物质分别小心地加入到大烧杯的水中.不断搅拌.一定能够使小烧杯中有固体析出的是 . A.冰 B.干冰 C.硝酸铵 D.浓硫酸 E.氢氧化钠 F.氧化钙
网址:http://m.1010jiajiao.com/timu3_id_30034[举报]
下列数据是硝酸钾固体在不同温度时的溶解度.
(1)硝酸钾溶液中的溶剂是 (填化学式)
(2)20℃时,向100g水中加入36g硝酸钾,充分溶解后得到 (填“饱和”或“不饱和”)溶液,这时溶液的溶质质量分数是 (保留一位小数)
查看习题详情和答案>>
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)20℃时,向100g水中加入36g硝酸钾,充分溶解后得到
 下列数据是硝酸钾固体在不同温度时的溶解度.
下列数据是硝酸钾固体在不同温度时的溶解度.| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
硝酸钾溶解度随温度升高而增大
硝酸钾溶解度随温度升高而增大
.(2)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到
饱和
饱和
(填“饱和”或“不饱和”)溶液.(3)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是
加水
加水
.(4)某标签上 标有“16%的硝酸钾溶液”,由该标签可获得的信息是
该溶液中溶质是硝酸钾、溶剂是水
该溶液中溶质是硝酸钾、溶剂是水
、该溶液中溶质与溶剂的质量比是16:100
该溶液中溶质与溶剂的质量比是16:100
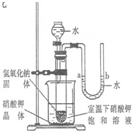
.(5)右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:将分液漏斗里适量的水加入大试管中,使足够量的氢氧化钠固体完全溶解后,能观察到的现象是
U型管中a液面下降b液面上升、烧杯中硝酸钾晶体部分溶解
U型管中a液面下降b液面上升、烧杯中硝酸钾晶体部分溶解
;请解释产生上述现象的主要原因是氢氧化钠固体溶于水放热,试管内温度升高,气体压强增大,导致液面变化,烧杯内溶液温度升高,硝酸钾溶解度随温度升高而增大,所以部分硝酸钾晶体溶解.
氢氧化钠固体溶于水放热,试管内温度升高,气体压强增大,导致液面变化,烧杯内溶液温度升高,硝酸钾溶解度随温度升高而增大,所以部分硝酸钾晶体溶解.
.下列数据是硝酸钾固体在不同温度时的溶解度.
(1)由上表可得到的信息是
(2)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到
(3)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是
(4)某标签上标有“16%的硝酸钾溶液”,由该标签可获得的信息是
查看习题详情和答案>>
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
硝酸钾的溶解度随着温度的升高而增大
硝酸钾的溶解度随着温度的升高而增大
.(2)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到
饱和
饱和
(填“饱和”或“不饱和”)溶液.(3)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是
升高温度
升高温度
.(4)某标签上标有“16%的硝酸钾溶液”,由该标签可获得的信息是
在100份质量的硝酸钾溶液中,含有16份质量的硝酸钾
在100份质量的硝酸钾溶液中,含有16份质量的硝酸钾
. 下列数据是硝酸钾固体在不同温度时的溶解度.
下列数据是硝酸钾固体在不同温度时的溶解度.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到________(填“饱和”或“不饱和”)溶液.
(3)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是________.
(4)某标签上 标有“16%的硝酸钾溶液”,由该标签可获得的信息是________、________.
(5)右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:将分液漏斗里适量的水加入大试管中,使足够量的氢氧化钠固体完全溶解后,能观察到的现象是________;请解释产生上述现象的主要原因是________. 查看习题详情和答案>>
 下列数据是硝酸钾固体在不同温度时的溶解度.
下列数据是硝酸钾固体在不同温度时的溶解度.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到________(填“饱和”或“不饱和”)溶液.
(3)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是________(填字母,下同).
A.升高温度 B.降低温度 C.再加硝酸钾固体 D.再加水
(4)如图所示,小烧杯中盛放的是饱和硝酸钾溶液.若将适量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,能够使小烧杯中有固体析出的是________.
A.冰 B.氧化钙 C.硝酸铵 D.氢氧化钠
(5)下列关于60℃时硝酸钾饱和溶液的说法,正确的是________
A.溶质质量最多为110g
B.溶质质量一定比溶剂多
C.一定比40℃硝酸钾溶液溶质的质量分数大. 查看习题详情和答案>>