1.下表是某城市空气质量日报公布的部分内容。对表中3个空气质量指标不会产生影响的是 ( )
|
项目 |
空气污染指数(API) |
空气质量级别 |
空气质量描述 |
|
可吸入颗粒物 |
52 |
Ⅱ |
良 |
|
二氧化硫 |
7 |
I |
优 |
|
二氧化氮 |
24 |
I |
优 |
A.焚烧垃圾 B.使用含磷洗衣粉
C.汽车排放的尾气 D.用煤和石油产品作燃料
23.(15分)某同学想通过下图装置(夹持装置已略去)实验,探究SO2与Na2O2反应的产物。
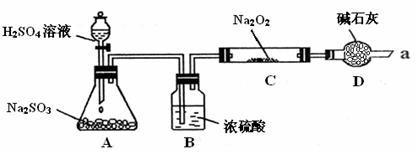
Ⅰ. 装置A中盛放浓硫酸的仪器名称是 ,其中发生反应的化学方程式为 。
Ⅱ. 如何检验反应中是否有O2生成 。
Ⅲ. 装置D除起了防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应作用外,还可以
。
Ⅳ. 对C中固体产物提出如下假设:
假设1:只有Na2SO3
假设2:只有Na2SO4
假设3: 。
⑴ 假设1的反应方程式:2SO2+ 2Na2O2= 。
⑵ 若Na2O2反应完全,为确定C中固体产物的成分,该同学设计如下,请您利用限选实验试剂帮助他完成该探究过程,并将答案写在相应位置。
限选实验试剂:酸性KMnO4溶液、Ba(NO3)2溶液、BaCl2溶液、1 mol/L HNO3溶液、4 mol/L盐酸。
|
实验操作 |
预期现象 |
结 论 |
|
步骤一:取少量C中固体产物于试管中,加入适量的蒸馏水溶解,然后将所得溶液分置于A、B试管中 |
固体完全溶解,得到无色透明溶液 |
|
|
步骤二:向A试管中滴加 ,振荡,观察溶液颜色变化。 |
|
假设1 或假设3成立;若没有该现象则假设2成立。 |
|
步骤三:向B试管中先滴加
, 再滴加 。 |
产生
, 再加入试剂看到产生白色沉淀。 |
假设3成立;若无白色沉淀产生则假设1成立。 |
⒘ 下列反应的离子方程式正确的是
A. AlCl3溶液中加入过量的浓氨水:Al3+ + 4NH3·H2O = AlO2- + 4NH4+ + 2H2O
B. 过量二氧化硫通入氢氧化钠溶液中:SO2 + OH- = HSO3-
C. 单质铜与稀硝酸反应:Cu + 2H+ + 2NO3- = Cu2+ + 2NO↑+ H2O
D. 氯化钡溶液与硫酸反应:Ba2+ + SO42- = BaSO4↓
⒙ 下列实验能达到预期实验目的的是
|
编号 |
实验内容 |
实验目的 |
|
A |
将在空气中放置已久的镁、铝两种元素的块状单质分别和热水作用,并滴入酚酞溶液 |
比较镁与铝的金属性强弱 |
|
B |
将Cl2通入NaBr溶液中 |
比较氯气与溴的氧化性强弱 |
|
C |
将CO2通入到Na2SiO3溶液中产生白色浑浊 |
比较C和Si的非金属性强弱 |
|
D |
将亚硫酸钠试样溶于适量的水中,再加入过量用稀硝酸酸化的氯化钡溶液 |
检验亚硫酸钠试样是否变质 |
⒚ 根据相关化学原理,下列判断一定正确的是
A. 含有共价键的化合物可能是离子化合物
B. A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
C. 若R2-和M+的电子层结构相同,则R原子的核电荷数比M原子的小
D. 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应
⒛ X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如右图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是
|
X |
Y |
|
|
|
Z |
W |
A. 原子半径:W > Z > Y > X
B. 最高价氧化物对应水化物的酸性:Z > W > X
C. Y的氢化物比Z的氢化物稳定
D. W单质能与水反应,生成一种具有漂白性的物质