1.吸氧腐蚀和析氢腐蚀的区别
|
电化腐蚀类型 |
吸氧腐蚀 |
析氢腐蚀 |
|
条件 |
水膜酸性很弱或呈中性 |
水膜酸性较强 |
|
正极反应 |
O2 + 4e- + 2H2O == 4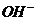 |
2H+ + 2e-==H2↑ |
|
负极反应 |
Fe -2e-==Fe2+ |
Fe -2e-==Fe2+ |
|
总反应方程式 |
4Fe(OH)2+O2+2H2O==4Fe(OH)3 2Fe(OH)3==Fe2O3+3H2O |
Fe + 2H+ = Fe2+
+ H2↑ |
|
腐蚀作用 |
是主要的腐蚀类型,具有广泛性 |
发生在某些局部区域内 |
 电解池是将电能转化为化学能的装置,在电解池中,阳极发生氧化反应、阴极发生还原反应,其放电顺序一般为:阳极:活泼性电极>
电解池是将电能转化为化学能的装置,在电解池中,阳极发生氧化反应、阴极发生还原反应,其放电顺序一般为:阳极:活泼性电极> >
>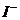 >
> >
> >
>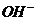 >含氧酸根离子阴极:与金属活动顺序表中金属阳离子的氧化顺序一致
>含氧酸根离子阴极:与金属活动顺序表中金属阳离子的氧化顺序一致
1.(惰性电极)电解电解质溶液的类型
|
类型 |
实例 |
电极反应特点 |
电解对象 |
电解质浓度 |
pH |
溶液复原 |
|
电解水 |
NaOH |
阴:2H++2e-====H2↑ 阳:4 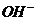 -4e-====2H2O+O2↑ -4e-====2H2O+O2↑ |
水 |
增大 |
增大 |
水 |
|
H2SO4 |
水 |
增大 |
减小 |
水 |
||
|
Na2SO4 |
水 |
增大 |
不变 |
水 |
||
|
电解电解质 |
HCl |
电解质电离出的阴阳离子分别在两极放电 |
电解质 |
减小 |
增大 |
氯化氢 |
|
CuCl2 |
电解质 |
减小 |
- |
氯化铜 |
||
|
放H2生碱 |
NaCl |
阴极:H2O放H2生碱阳极: 电解质阴离子放电 |
电解质 和水 |
生成新电解质 |
增大 |
 氯化氢 氯化氢 |
|
放O2生酸 |
CuSO4 |
阴极:电解质阳离子放电 阳极:H2O放O2生酸 |
电解质 和水 |
生成新电解质 |
减小 |
氧化铜 |
 Cu2O是一种半导体材料,基于绿色化学理念设计的制取.Cu2O的电解池示意图如下,点解总反应:2Cu+H2O==Cu2O+H2O
Cu2O是一种半导体材料,基于绿色化学理念设计的制取.Cu2O的电解池示意图如下,点解总反应:2Cu+H2O==Cu2O+H2O 。下列说法正确的是
。下列说法正确的是

 ,不能实现该反应的电池是( )
,不能实现该反应的电池是( ) B.
B.
 D.
D.
 =
=  =
=

 ,把二价镍氧化为三价镍。以下说法正确的是( )
,把二价镍氧化为三价镍。以下说法正确的是( )
 CuSO4+H2↑
CuSO4+H2↑ )=3:3:2:1,电解过程明显分为三个阶段:
)=3:3:2:1,电解过程明显分为三个阶段:



 (3)四氯化碳萃取法工艺复杂、设备投资大;经济效益低、环境污染严重
(3)四氯化碳萃取法工艺复杂、设备投资大;经济效益低、环境污染严重 H2↑
H2↑ Mn+,电子直接转移给氧化剂
Mn+,电子直接转移给氧化剂

 Fe2+
B.2H++2e-
Fe2+
B.2H++2e-



 2NaOH+H2↑+Cl2↑(反应条件:直流电)
2NaOH+H2↑+Cl2↑(反应条件:直流电) 正极:
正极:
 正极:
正极:






 正极:
正极:

