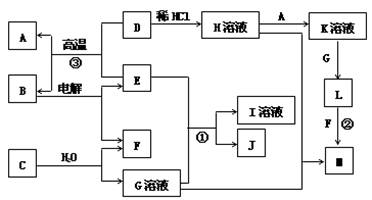
27.(16分)食盐是日常生活的必需品,也是重要的化工原料。
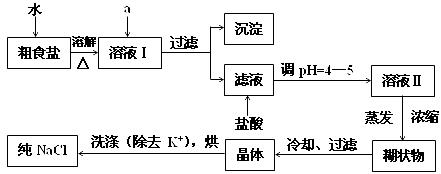
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和Na2CO3溶液,饱和K2CO3溶液,NaOH溶液,BaCl2溶液,Ba(NO3)2
溶液,75%乙醇,四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为____________________________(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_______________________。
(2)用提纯的NaCl配制500mL 4.00 mol·L-1的NaCl溶液,所用仪器除药匙、玻璃棒外
|
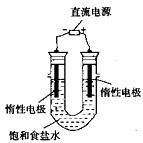
(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2______(填“>”“=”或“<”)2L,原因是_________________________。装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法为____________________。
(4)实验室制备H2和Cl2通常采用下列反应:Zn + H2SO4===ZnSO4 + H2↑;
MnO2 + 4HCl(浓)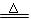 MnCl2
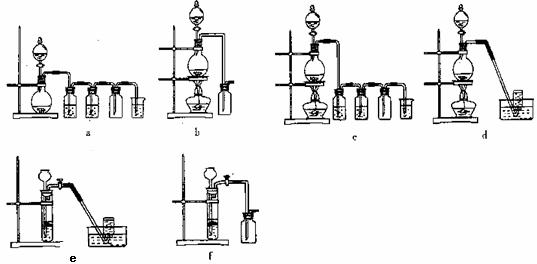
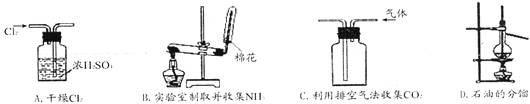
+ Cl2↑+ 2H2O,据此,从下列所给仪器装置中选择制备并收集H2的装置_______(填代号)和制备并收集干燥、纯净Cl2的装置________(填代号)。
MnCl2
+ Cl2↑+ 2H2O,据此,从下列所给仪器装置中选择制备并收集H2的装置_______(填代号)和制备并收集干燥、纯净Cl2的装置________(填代号)。
可选用制备气体的装置:
选考题(每科选做1题)
 Al(OH)3+3H+
Al(OH)3+3H+ H1= +156.6 kJ·mol-1
H1= +156.6 kJ·mol-1 HCO3- + H+的平衡常数K1=_________。(已知:10-5.60=2.5×10-6)
HCO3- + H+的平衡常数K1=_________。(已知:10-5.60=2.5×10-6)