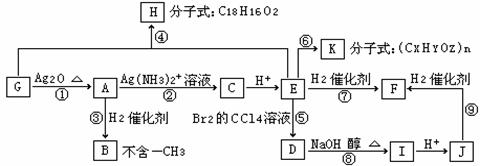
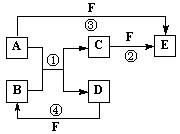
27.(20分)请按要求填空:
Ⅰ.下列实验操作或对实验事实的叙述正确的是 (填序号)。
①用稀HNO3清洗做过银镜反应实验的试管;
②在中学《硫 酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次;
酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次;
③用碱式滴定管量取20.00 mL 0.1000 mol·L-1 KMnO4溶液;
④除去FeCl3酸性溶液中少量的FeCl2:加入稍过量双氧水后放置;
⑤不慎将苯酚溶液沾到皮肤上,立即用酒精清洗;
⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物;
⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体;
⑧除去CO中少量O2:通过灼热的Cu网后收集气体;
⑨除去苯中溶有的少量苯酚:加入适量浓溴水反应后过滤;
Ⅱ.某实验小组用废铁屑或废铁丝与稀硫酸在加热条件下制取FeSO4·XH2O,并测定该晶体中结晶水含量。
(1)铁屑表面少量的铁锈(主要成分为Fe2O3·AH2O)对制取硫酸亚铁有无影响?其原因是什么?
(2)FeSO4在不同温度下的溶解度如下表所示
温度/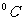 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
溶解度/g |
18.5 |
20.8 |
26.3 |
32.8 |
40.1 |
48.4 |
52.4 |
50.9 |
43.7 |
由于废铁屑含有C、S等杂质,为了使FeSO4溶液的浓度增大,便于反应后分离溶液和残渣,拟采用水浴加热和趁热过滤的方法。实验时,水浴温度最好控制在 ℃左右。
(3)测定晶体中结晶水含量所用的实验仪器除托盘天平、研钵、坩埚钳、三脚架、酒精灯、药匙外,还有 ;判断晶体中的结晶水完全失去的实验操作是 。
(4)计算FeSO4晶体化学式中X的表达式为X= (已知FeSO4晶体的质量为wg,FeSO4晶体中结晶水的质量为mg)
(5)由于铁屑或铁丝与硫酸反应速率慢,实验过程中有人提出采用电解的方法,可以加快制取FeSO4溶液的反应速率,该方法的电解质溶液是 ,阳极的电极反应式为 。