[例1]A、B、C、D、E、F为原子序数依次增大的主族元素,已知A、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,D元素原子的最外层电子比次外层电子数少4,E元素原子次外层电子数比最外层电子数多3。请回答:
①写出下列元素的符号:A________,D________,E________。
②用电子式表示B、F形成化合物的过程____________________________________________。
③A、C两种元素最高价氧化物的水化物反应的离子方程式:___________________________。
④D的固态氧化物是________晶体,含n mol D的氧化物的晶体中含D-O共价键为________mol。
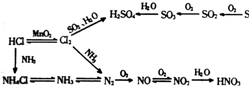
 [例2]X、Y、Z为常见的三种单质。常温下X是固体,Y是液体,Z是无色气体。其反应关系如图12-1所示.其中B的溶液显强酸性。
[例2]X、Y、Z为常见的三种单质。常温下X是固体,Y是液体,Z是无色气体。其反应关系如图12-1所示.其中B的溶液显强酸性。
请回答下列问题:
(1)根据上述关系,确定X、Y、Z的化学式:X________,Y________,Z________。
(2)Y元素在元素周期表中的位置为________。
(3)写出A溶于水后加入X的离子方程___________________________________________。
(4)写出C的溶液中通入过量氯气的离子方程____________________________________。
[例3]X、Y、Z为三个不同短周期非金属元素的单质。
在一定条件下有如下反应:Y+X→A(气),Y+Z→B(气)。请针对以下两种不同情况回答:
(1)若常温下X、Y、Z均为气体,且A和B化合生成固体C时有白烟产生,则:
①Y的化学式是____________;
②生成固体C的化学方程式是_________________________。
(2)若常温下,Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
①B的化学式是________________:
②向苛性钠溶液中通入过量的A,所发生反应的离子方程式是:________________________。
③将Y与(1)中某单质的水溶液充分反应可生成两种强酸,
该反应的化学方程__________________________________________________________。
[例4]A、B、C、D是四种可溶的化合物,分别由阳离子K+、Ba2+、A13+、Fe3+和阴离子OH-、CO23-、NO3-、SO42-两两组合而成,它们的溶液发生如下反应:
A与B反应生成白色沉淀,再加过量A,沉淀量减少,但不会完全消失;
C与D反应生成有色沉淀: B与C反应生成白色沉淀。
写出它们的化学式:A:__________ B:__________C:__________ D:__________
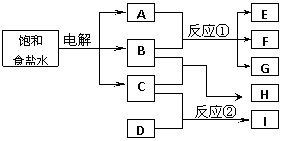 [例5]下图每一方框中的字母代表一种反应物或生成物:
[例5]下图每一方框中的字母代表一种反应物或生成物:
|
|
C |
D |
I |
|
起始组成/mol |
6 |
4 |
0 |
|
某时刻组成/mol |
3 |
3 |
2 |
物质A跟B反应生成物质E、F和G;物质C跟D反应生成物质I,某温度下该反应起始和某时刻的反应混合物组成如右上表格所示。请填写下列空白:
①物质H的化学式是________________________________;
②反应①的化学方程式是_______________________________________________________;
③反应②的化学方程式(须注明反应条件)是________________________________________。
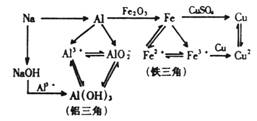
 A、B、C是常见单质,X、Y、Z是氧化物,它们之间有如图所示转化关系:
A、B、C是常见单质,X、Y、Z是氧化物,它们之间有如图所示转化关系: 图中A-L所代表的各物质是中学化学里常见的物质,已知B、J是单质。A是化合物;E的溶液跟苯酚溶液混合,溶液呈紫色。A-L各物质之间相互反应转化的关系如图所示(未注明必要的反应条件)
图中A-L所代表的各物质是中学化学里常见的物质,已知B、J是单质。A是化合物;E的溶液跟苯酚溶液混合,溶液呈紫色。A-L各物质之间相互反应转化的关系如图所示(未注明必要的反应条件) 如图所示的物质的转化关系中,A是一种固体单质,E是一种白色沉淀。据图填写。
如图所示的物质的转化关系中,A是一种固体单质,E是一种白色沉淀。据图填写。 图中每个方框表示有关的一种反应物或生成物,方框中字母是物质代号,已知B、D、E、F、X均为单质,判断并回答下列问题:
图中每个方框表示有关的一种反应物或生成物,方框中字母是物质代号,已知B、D、E、F、X均为单质,判断并回答下列问题: 从某物质A的水溶液出发有如图所示的转化关系
从某物质A的水溶液出发有如图所示的转化关系