17.(8分)在一容积为2 L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g ) △H<0 反应中NH3的物质的量浓度的变化的情况如下图:
2NH3(g ) △H<0 反应中NH3的物质的量浓度的变化的情况如下图:
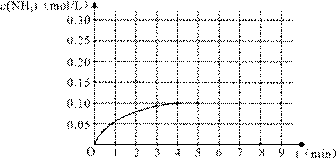
(1)根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)为______ _。
(2)该反应的化学平衡常数表达式K____ _ 。
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为________。
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
(4)反应达到平衡后,第5分钟末,保持其它条件不变,若只把容器的体积缩小一半,平衡_________________________移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________________(填“增大”、“减小”或“不变”)。
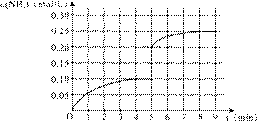
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25 mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
|
17 |
(1) |
0.025 mol/L·min |
1分 |
单位不写或写错扣0.5分 |
|
(2) |
略 |
1分 |
|
|
|
(3) |
a、c |
2分 |
答对一个给1分;答错一个扣一分 |
|
|
(4) |
向正反应方向 |
1分 |
|
|
|
不变 |
1分 |
|
||
|
(5) |
 |
2分 |
|
24、(潮州二模)(14分)
(1) (6分)在一定条件下,在一容积可变的密闭容器中,将SO2和O2混合发生反应:
2SO2(g)+O2(g) 2SO3(g) ΔH=-92.3KJ/mol
2SO3(g) ΔH=-92.3KJ/mol
0-4min时,容器气体压强为101KPa。反应过程中,SO2、O2、SO3的物质的量(mol)的变化如下表:
|
时间min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
n(SO2) |
2.00 |
1.92 |
1.84 |
1.76 |
1.76 |
1.64 |
1.52 |
1.40 |
1.40 |
1.40 |
|
n(O2) |
1.00 |
0.96 |
0.92 |
0.88 |
0.88 |
0.82 |
0.76 |
0.70 |
0.70 |
0.70 |
|
n(SO3) |
0 |
0.08 |
0.16 |
0.24 |
0.24 |
0.36 |
0.48 |
0.60 |
0.60 |
0.60 |
回答下列问题:
① 时,反应处于平衡状态。
②第5min时,从速率和转化率两个方面分析,改变的外界条件是 ;平衡向 方向移动。
 ③在0.1Mpa、500℃时,起始时O2和SO2的物质的量之比
③在0.1Mpa、500℃时,起始时O2和SO2的物质的量之比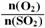 的值,与SO2平衡时的体积百分含量的变化曲线如图。
的值,与SO2平衡时的体积百分含量的变化曲线如图。
在图中画出在相同压强下,温度为400℃时,起始O2和SO2的物质的量之比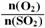 的值,与SO2平衡时的体积百分含量的大致变化曲线。
的值,与SO2平衡时的体积百分含量的大致变化曲线。
(2) (8分)草酸(H2C2O4)是二元弱酸,KHC2O4溶液呈酸性。向10mL 0.01mol•L―1的H2C2O4溶液滴加0.01mol•L―1KOH溶液V(mL),回答下列问题。
①当V<10mL时,反应的离子方程式为 。
②当V=10mL时,溶液中HC2O4―、C2O42―、H2C2O4、H+的浓度从大到小的顺序为
。
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(C2O42―)+c(HC2O4―);
当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(C2O42―)+c(HC2O4―)+c(H2C2O4);则a b(填“<”,“=”或“>”)。
④当V=20mL时,再滴入NaOH溶液,则溶液中n(K+) / n(C2O42-)的值将 (填“变大”,“变小”,“不变”),原因是 。
 2NH3(g) ΔH=-92 kJ·mol-1。
2NH3(g) ΔH=-92 kJ·mol-1。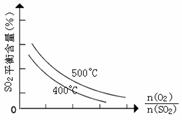
 HC2O4-+OH―,当增大c(OH―)时,平衡向逆方向移动,n(C2O42-)的值变大,而n(K+)的值不变,故n(K+) / n(C2O42-)的值变小。(2分)
HC2O4-+OH―,当增大c(OH―)时,平衡向逆方向移动,n(C2O42-)的值变大,而n(K+)的值不变,故n(K+) / n(C2O42-)的值变小。(2分) ;(3)ⅰ 减小,升温(或通入A气体);ⅱ:任意值。
;(3)ⅰ 减小,升温(或通入A气体);ⅱ:任意值。 2C(g)(⊿H<0)
2C(g)(⊿H<0) 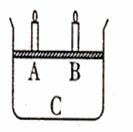 (3)如右图所示,将4mol气体A和2mol气体B混合后置于体积可变的等压容器中,一定温度下达到平衡状态X时,测得气体总物质的量为4.2mol。若A、B、C起始的物质的量分别用a、b、c表示。试回答:
(3)如右图所示,将4mol气体A和2mol气体B混合后置于体积可变的等压容器中,一定温度下达到平衡状态X时,测得气体总物质的量为4.2mol。若A、B、C起始的物质的量分别用a、b、c表示。试回答: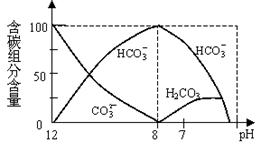 ②当pH=7时,溶液中各种离子其物质的量浓度之间的等量关系是:
。
②当pH=7时,溶液中各种离子其物质的量浓度之间的等量关系是:
。 HS- + OH-(2分)
HS- + OH-(2分)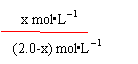 (2.0-x) mol•L-1 x mol•L-1
(2.0-x) mol•L-1 x mol•L-1
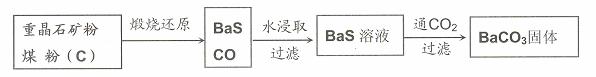
 O2(g)=CO(g);△H= -110.5 kJ·mol-1
O2(g)=CO(g);△H= -110.5 kJ·mol-1 BaCO3(s)+SO42―(aq)(平衡常数K=0.042)
BaCO3(s)+SO42―(aq)(平衡常数K=0.042) 2NO2(g);△H=
+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g);△H=
+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )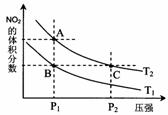 A.A、C两点的反应速率:A>C
A.A、C两点的反应速率:A>C