18.(每空2分,共8分)氮是地球上含量最丰富
的一种元素,氮及其化合物在工农业生产、生
活中有着重要作用。请回答下列问题:
(1)右图是1mol NO2和1mol CO反应生成CO2
和NO过程中能量变化示意图,请写出NO2
和CO反应的热化学方程式 。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:
N2(g)+3H2(g) 2NH3(g)△H<O,其化学平衡常数K与温度t的关系如下表:
2NH3(g)△H<O,其化学平衡常数K与温度t的关系如下表:
|
t/℃ |
200 |
300 |
400 |
|
K |
K1 |
K2 |
0.5 |
请完成下列问题;
①试比较K1、K2的大小,K1____K2(填写“>”、“=”或“<”);
②400℃时,反应2NH3(g) N2(g)+3H=2(g)的化学平衡常数的值为_
___。
N2(g)+3H=2(g)的化学平衡常数的值为_
___。
当测得NH3和N2、H2的物质的量分别为3mol和2mol、1mol时,则该反应的v(N2)(正)____v(N2)(逆)(填写“>”、“=”或“<”)。
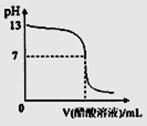 常温下,向10mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1醋酸溶液,所得滴定曲线如下图所示。下列说法正确的是 ( )
常温下,向10mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1醋酸溶液,所得滴定曲线如下图所示。下列说法正确的是 ( ) CO32-+H3O+
CO32-+H3O+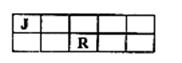 J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右下表。已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列说法错误的是 ( )
J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右下表。已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列说法错误的是 ( )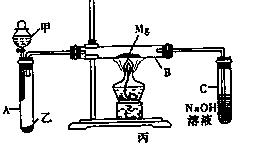

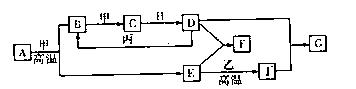
 (3)将Y的低价氧化物通人W的最高价氧化物对应水化物中,经充分反应后,所得溶液呈中性,则混合溶液中的溶质主要为
;溶液中c(W+)=
。
(3)将Y的低价氧化物通人W的最高价氧化物对应水化物中,经充分反应后,所得溶液呈中性,则混合溶液中的溶质主要为
;溶液中c(W+)=
。